INTRODUCTION
L’héparine non fractionnée (HNF) demeure un anticoagulant parentéral nécessaire dans de nombreuses situations cliniques aiguës lorsque les héparines de bas poids moléculaire (HBPM) sont jugées inadaptées, notamment en soins intensifs, en cardiologie interventionnelle, en chirurgie cardiaque, dans la prise en charge des épisodes de maladie thromboembolique veineuse et chez les patients sous assistance circulatoire extracorporelle avec oxygénation. En effet ses propriétés pharmacologiques, incluant une demivie courte, une compatibilité avec l’insuffisance rénale et la disponibilité d’un antidote, expliquent la persistance de son utilisation malgré le développement des HBPM et des anticoagulants oraux directs. Toutefois, l’HNF présente une variabilité intra- et interindividuelle importante de réponse au traitement ainsi qu’un index thérapeutique étroit, exposant les patients à un risque thrombotique en cas de sous-dosage ou hémorragique en cas de surdosage. Cette variabilité impose un suivi rigoureux au laboratoire afin d’assurer l’efficacité et la sécurité du traitement. Historiquement fondé sur le temps de céphaline activée (TCA), le suivi s’appuie également sur la mesure d’activité anti-Xa (1).
Ces dernières années, le développement de l’automatisation et le renforcement des contrôles qualité ont contribué à une meilleure maîtrise de la phase analytique. À l’inverse, la phase préanalytique reste insuffisamment standardisée et maîtrisée et constitue une source majeure de variabilité pouvant altérer la qualité et l’interprétation des résultats analytiques. Le prélèvement sanguin peut induire une activation plaquettaire in vitro, favorisée par le traumatisme, le cisaillement et les variations de température. Cette activation entraîne la libération du facteur plaquettaire 4 (FP4), une protéine à forte affinité pour l’héparine, capable d’en neutraliser l’activité anticoagulante. Cette interaction peut conduire à une diminution artéfactuelle des valeurs de TCA et de l’activité anti-Xa, notamment lorsque la centrifugation ou l’analyse est retardée ou lorsque les conditions de transport et de conservation sont mal adaptées. Même après séparation du plasma, des phénomènes de neutralisation de l’héparine peuvent survenir, soulignant le caractère temps-dépendant du suivi de l’HNF. Ces phénomènes revêtent une importance particulière dans les laboratoires modernes, où les durées de la phase préanalytique peuvent varier selon les modalités de transport des échantillons, la centralisation des plateformes analytiques et les contraintes organisationnelles des laboratoires.
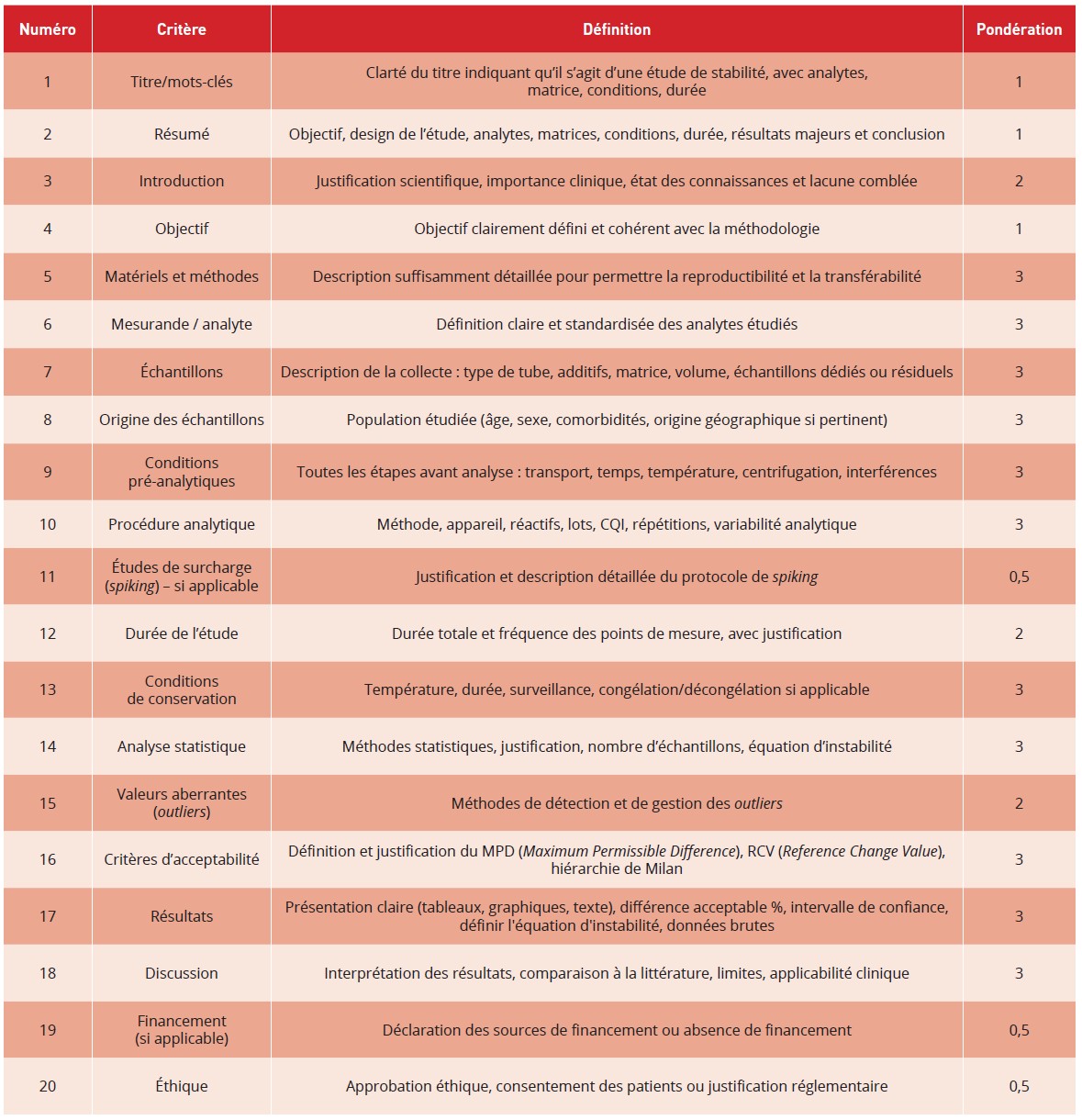
Les variations préanalytiques peuvent entraîner une sousestimation de l’activité anticoagulante de l’HNF, conduisant à des ajustements thérapeutiques inappropriés et à une augmentation du risque d’événements indésirables. Les recommandations actuelles préconisent une centrifugation aussi rapide que possible après le prélèvement suivie d’une analyse dans les plus brefs délais, mais elles reposent sur un nombre limité d’études, souvent hétérogènes et présentant des limites méthodologiques. Afin d’améliorer la qualité et la comparabilité des études de stabilité, la European Federation of Clinical Chemistry and Laboratory Medicine (EFLM) a proposé en 2020 la checklist CRESS (Checklist for Reporting Stability Studies), qui comprend 20 critères couvrant la description des échantillons, des conditions préanalytiques, des méthodes analytiques, des conditions de stockage et des analyses statistiques (Tableau 1) (2). Cette checklist a pour objectif de standardiser la conception et la publication des études de stabilité afin d’améliorer la reproductibilité, la transposabilité et la pertinence clinique de ces études. Dans ce contexte, cette revue propose une analyse critique des données disponibles relatives à la stabilité du TCA et de l’activité anti-Xa dans le cadre du suivi de l’HNF à dose thérapeutique, en fonction des conditions préanalytiques. La qualité méthodologique des études ainsi que la pertinence et l’exhaustivité des données fournies ont été évaluées selon les critères CRESS, afin d’identifier leurs limites.
MATÉRIEL ET MÉTHODES
Recherche bibliographique et sélection des études
Une recherche bibliographique extensive suivie d’une procédure d’extraction des données a été réalisée. La base de données PubMed (Medline) a été interrogée à l’aide des mots-clés et termes MeSH suivants : « activated partial thromboplastin time », « stability », « anti-Xa measurement », « pre-analytical phase », « citrate », « CTAD » et « unfractionated heparin ». Aucune restriction de date n’a été appliquée, et la recherche a été actualisée pour la dernière fois en janvier 2026. Les listes de références des articles pertinents ont également été examinées afin d’identifier des publications supplémentaires. Les articles de revue et les recommandations ont seulement été consultés afin de repérer d’éventuelles études pertinentes non identifiées lors de la recherche initiale. Les données pertinentes ont été extraites à l’aide d’un tableau prédéfini. La sélection des articles et l’extraction des données ont été réalisées de manière indépendante par trois des auteurs (AD, TL et FM), et les désaccords réglés par discussion et consensus.
RÉSULTATS
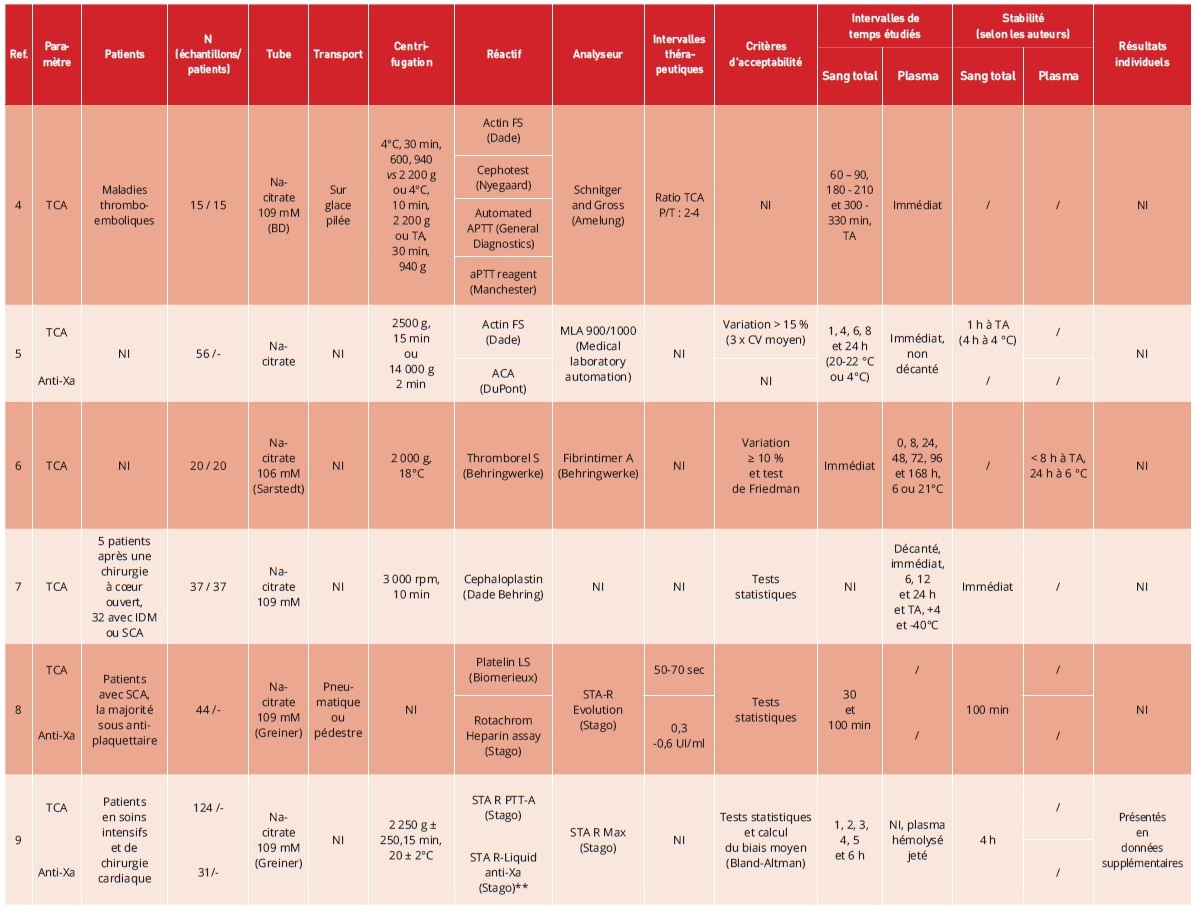
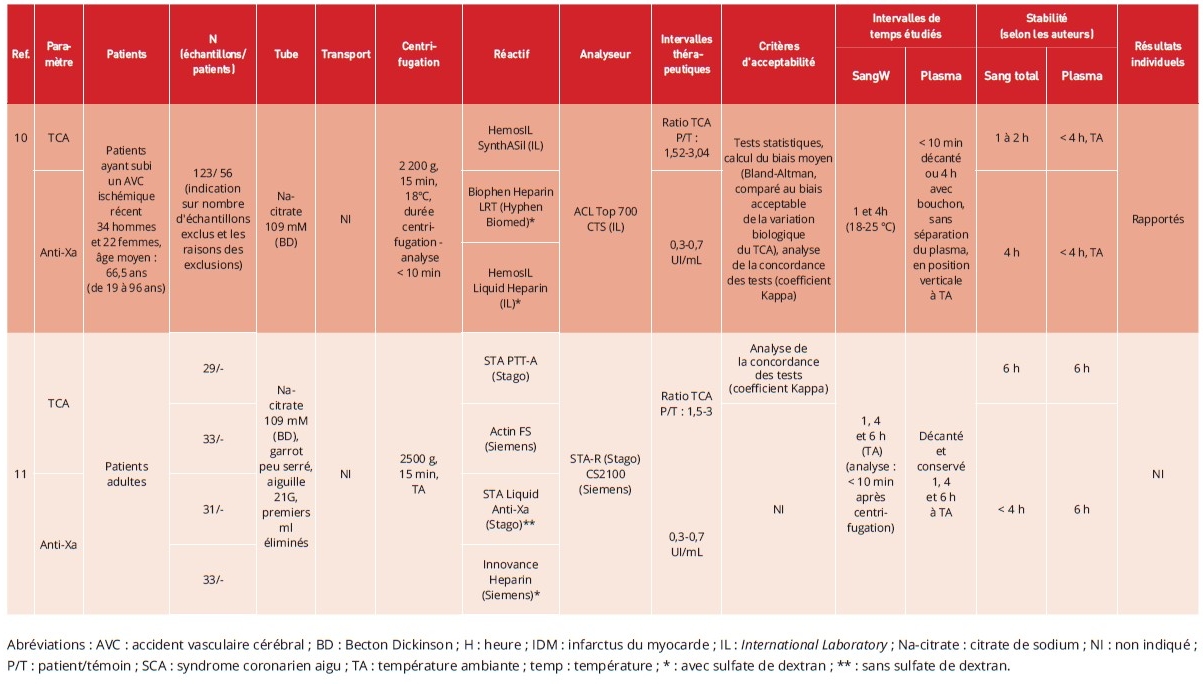
Depuis 1983, neuf études publiées ont évalué la stabilité du TCA et/ou de l’activité anti-Xa au cours du temps dans des échantillons sanguins prélevés dans des tubes avec citrate et/ou CTAD (3-11), dont une seule étude prospective (9) (Tableaux 2 et 3). Parmi ces études, trois n’ont évalué que le TCA (4,6,7), les autres ont évalué en parallèle la stabilité du TCA et de l’activité anti-Xa.
Nombre et origine des échantillons
Seules quatre études précisent l’indication clinique ayant conduit à l’instauration d’un traitement par HNF chez les patients prélevés, et une seule étude rapporte des données démographiques des patients, telles que l’âge moyen et la répartition selon le sexe (10). Par ailleurs, bien que le nombre d’échantillons analysés varie de 15 à 126 selon les études, le nombre de patients inclus n’est pas toujours clairement indiqué. Enfin, l’inclusion de patients recevant un traitement antiplaquettaire concomitant à l’HNF dans l’une des études constitue un facteur de confusion potentiel (8).
Types de tube de prélèvement
Les tubes contenant du citrate de sodium sont les plus utilisés en pratique courante pour la réalisation des explorations de la coagulation. Les tubes CTAD (citrate, théophylline, adénosine, dipyridamole) ont été spécifiquement développés afin de limiter l’activation plaquettaire in vitro et, par conséquent, réduire la libération du FP4. Dans la majorité des études, la concentration en citrate ainsi que le fabricant des tubes sont clairement documentés.
Cinq études ont évalué la stabilité du TCA et du niveau
Tableau 1 : Liste des 20 critères CRESS (Checklist for Reporting Stability Studies) utilisée pour évaluer la qualité des études de stabilité en biologie médicale, telle que définie par l’EFLM WG-PRE. Chaque critère est évalué selon quatre niveaux de qualité (de 1 à 4).
Table 1: List of the 20 CRESS criteria (Checklist for Reporting Stability Studies) used to assess the quality of stability studies in laboratory medicine, as defined by the EFLM WG-PRE. Each criterion is evaluated according to four quality levels (from 1 to 4).
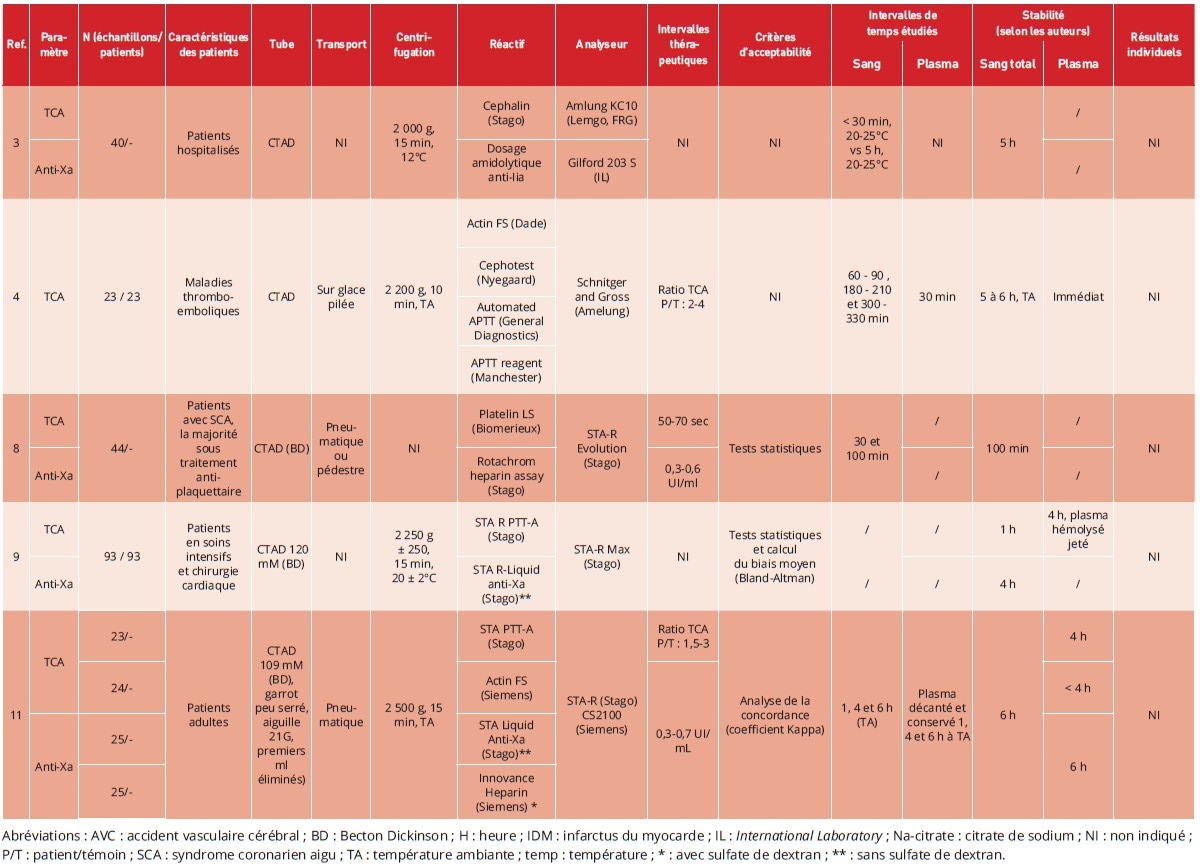
d’héparine en évaluant l’activité anti-Xa chez des patients traités par HNF, à partir de prélèvements réalisés avec des tubes CTAD (Tableau 3) (3,4,8,9,11). Dans l’ensemble, ces études montrent qu’au cours du temps, les résultats des deux tests mesurés avec les tubes citrate sont significativement plus bas que ceux obtenus avec les tubes CTAD. Toutefois, cette différence est très variable selon les prélèvements et selon les études. Dans l’étude de Ray et coll., l’écart médian entre les échantillons prélevés dans des tubes citrate et ceux prélevés dans des tubes CTAD, 30 minutes après le prélèvement, était pour le TCA de 9,3 secondes (écart interquartile (EIQ) : 4,4-13,4 ; de 1,1 à 43 secondes) et pour l’activité anti-Xa de 0,07 UI/mL (EIQ : 0,05-0,12 ; de 0,03 à 0,18 UI/mL) (8) alors que dans l’étude de Billoir et coll., la différence moyenne entre les deux types de tubes au-delà de 2 heures après le prélèvement était de 1,24 ± 10,9 secondes pour le TCA et de 0,025 ± 0,041 UI/mL pour l’activité anti-Xa (9). Ray et coll. ont observé que le recueil des échantillons dans des tubes CTAD réduisait significativement la libération plaquettaire de FP4, comparativement aux échantillons collectés dans des tubes contenant uniquement du citrate, et ce indépendamment des durées de conservation étudiées (30 et 100 minutes en sang total) (8). Pour le sang total, trois études concluent à une stabilité acceptable du TCA et de l’activité anti-Xa jusqu’à 5 à 6 heures entre le prélèvement en tube CTAD et la centrifugation (3,4,11). En revanche, Ray et coll. ainsi que Billoir et coll. ont rapporté des durées de stabilité plus courtes, respectivement de 100 minutes et 1 heure pour le TCA, et de 100 minutes et 4 heures pour l’activité anti-Xa (8,9). Il convient de souligner que, dans l’étude de Ray et coll., la stabilité n’a pas été évaluée au-delà de 100 minutes (8). Concernant les analyses réalisées avec du plasma issu de sang CTAD, van den Besselaar et coll. recommandent une analyse immédiate du TCA après centrifugation ; Billoir et coll. et Gremillet et coll. considèrent la stabilité bonne jusqu’à 4 heures après le prélèvement (4,9,11). Pour l’activité anti-Xa mesurée en plasma, seule l’étude de Gremillet et coll. a évalué cette condition avec des tubes CTAD et rapporte une stabilité d’au moins 6 heures après le prélèvement (11). Dans cette étude, le coefficient Kappa comparant les résultats du TCA obtenus avec des plasmas centrifugés à 1 heure et à 6 heures après le prélèvement était de 1,0 avec le réactif Siemens, indiquant une concordance excellente. En revanche, avec le réactif Stago, le coefficient Kappa était de 0,63, correspondant à une concordance seulement modérée et révélant l’existence de discordances pour une partie des échantillons entre 1 heure et 6 heures après le prélèvement. Par ailleurs, les études de Billoir et coll. et Gremillet et coll. ont rapporté une stabilité dans l’ensemble comparable du TCA et de l’activité anti-Xa entre les tubes citrate et CTAD, tant pour le sang total que pour le plasma, à l’exception du TCA mesuré en plasma avec le réactif PTT-A (Stago), pour lequel une stabilité paradoxalement plus longue a été observée dans les tubes citrate (6 heures) comparés aux tubes CTAD (4 heures) pour l’étude de Gremillet et coll. (9,11).
Transport des échantillons au laboratoire
Deux études seulement précisent que les échantillons ont été acheminés au laboratoire par un système de transport pneumatique, sans en décrire les caractéristiques techniques alors que des contraintes mécaniques générées par les accélérations, décélérations, vibrations et forces de cisaillement au cours de ce type de transport sont susceptibles d’induire une activation plaquettaire in vitro (8,11). Une étude qui a comparé les valeurs de TCA obtenues à partir de 11 échantillons transportés soit par système pneumatique (sans précision sur les caractéristiques du système), soit par transport manuel, est plutôt rassurante puisqu’elle n’a pas mis en évidence de différence significative entre ces deux modalités (8). Par ailleurs, une étude indique que les échantillons ont été transportés sur glace pilée, alors même que l’exposition des plaquettes sanguines au froid peut induire une activation plaquettaire in vitro (4).
Modalités de centrifugation
Cinq études rapportent les paramètres de centrifugation utilisés, incluant la vitesse, la température et la durée. Dans l’étude de van den Besselaar et coll., les échantillons provenant de patients traités par HNF et centrifugés à 600 g présentaient des valeurs de TCA légèrement plus courtes que ceux centrifugés à 940 g et 2 200 g, sans que ces différences atteignent la significativité statistique (4). Il convient toutefois de souligner que la durée de centrifugation appliquée dans cette étude était inhabituelle puisque de 30 minutes.
Réactifs
Dans l’ensemble des études analysées, les réactifs utilisés pour l’évaluation de la stabilité du TCA et/ou de l’activité
Tableau 2 : Synthèse des études et données disponibles sur la stabilité pré-analytique du TCA et/ou de l’activité anti-Xa dans des échantillons collectés en tubes citrate chez des patients traités par HNF à dose thérapeutique.
Table 2: Summary of available studies and data on the pre-analytical stability of TCA and/or anti-Xa activity in samples collected in citrate tubes from patients treated with therapeutic doses of HNF.
Tableau 3 : Synthèse des études et données disponibles sur la stabilité préanalytique du TCA et/ou de l’activité anti-Xa dans des échantillons collectés en tubes CTAD chez des patients traités par HNF à dose thérapeutique.
Table 3: Summary of available studies and data on the preanalytical stability of TCA and/or anti-Xa activity in samples collected in CTAD tubes from patients treated with therapeutic doses of HNF.
anti-Xa sont précisément décrits, avec mention du nom commercial, du fabricant et de l’analyseur utilisé. Dans l’étude de van den Besselaar et coll., quatre réactifs de TCA (Actin-FS, APTT-A, Cephotest et aPTT Manchester reagent) ont été évalués (4). La conservation de sang citraté non centrifugé à température ambiante pendant 1 à 5 heures a entraîné un raccourcissement du TCA compris entre 15 % et 29 %, selon le réactif utilisé. Une autre étude a comparé l’influence de deux réactifs de TCA sur la stabilité de ce paramètre et a montré que le plasma restait stable jusqu’à 6 heures lorsque le TCA était mesuré à l’aide du réactif STA® PTT-A (Stago), contre moins de 4 heures avec le réactif Actin® FS (Siemens), lorsque le prélèvement était réalisé sur tube citrate (11).
Concernant les tests d’activité anti-Xa, la principale différence entre les réactifs réside dans la présence ou l’absence de sulfate de dextran. Ce dernier dissocie l’héparine des protéines neutralisantes, notamment le FP4 libéré lors de l’activation plaquettaire, ce qui limite la sous-estimation de l’activité anti-Xa et améliore la stabilité in vitro des échantillons. Cependant, le sulfate de dextran peut également dissocier l’héparine de la protamine, utilisée en chirurgie cardiaque pour neutraliser l’héparine, entraînant une augmentation artificielle des valeurs d’activité anti-Xa et une surestimation de l’activité anticoagulante réelle (12,13). Une étude ayant comparé la stabilité de l’activité anti-Xa mesurée à l’aide de réactifs contenant ou non du sulfate de dextran n’a pas mis en évidence de différence significative, que ce soit sur plasma ou sur sang total prélevé sur tubes citrate ou CTAD (11). Toutefois, l’absence de disponibilité des données individuelles limite l’interprétation de ces résultats et ne permet pas de tirer de conclusions définitives.
Intervalles thérapeutiques
Parmi les neuf études incluses, seules quatre précisent les intervalles thérapeutiques du TCA et/ou de l’activité anti-Xa appliqués au sein du laboratoire (4,8,10,11). Van den Besselaar et coll. et Toulon et coll. indiquent que les intervalles thérapeutiques du TCA correspondaient à des activités anti-Xa comprises, respectivement, entre 0,3 et 0,8 UI/mL et 0,3 et 0,7 UI/mL (4,10).
Critères d’acceptabilité
Les critères d’acceptabilité définissant la stabilité des paramètres au cours du temps ainsi que les méthodes statistiques employées sont rarement précisés et, lorsqu’ils le sont, sont extrêmement différents d’une étude à l’autre. En outre, ces critères ne reposent généralement pas sur des considérations cliniques, à l’exception de l’étude de Toulon et coll. (10).
L’intégration de la variabilité biologique, notamment à l’aide de paramètres tels que la valeur de changement de référence (RCV, Reference Change Value), définie comme la variation minimale entre deux résultats successifs permettant de conclure à une modification réelle plutôt qu’à une simple fluctuation biologique ou analytique, contribuerait à une meilleure évaluation de la pertinence clinique des variations observées. L’absence de cette approche dans la majorité des études limite la comparabilité des résultats ainsi que leur interprétation clinique (14). De plus, la taille des échantillons analysés par condition devrait être justifiée par une hypothèse sur les variations cliniquement acceptables, en nombre (reclassement) et en amplitude extrême. Il n’est toutefois pas facile de déterminer sur des bases aussi solides que possible cette acceptabilité en termes cliniques. À noter que les données individuelles sont disponibles seulement pour les études de Billoir et coll. et de Toulon et coll. (9,10).
Durées maximales en sang total (du prélèvement jusqu’à la centrifugation) selon les auteurs
Différentes durées entre le prélèvement et la centrifugation ont été étudiées, allant d’une prise en charge immédiate jusqu’à 24 heures. En tube citrate, Adcock et coll. ont rapporté une stabilité du TCA en sang total pendant 1 heure à température ambiante, avec un raccourcissement significatif de 45 % après 4 heures, corrélé à une augmentation du FP4, mais cette étude n’a inclus que trois patients (5). Adwad et coll. recommandent également une centrifugation immédiate, rapportant un allongement significatif du TCA à 6 heures, sans point intermédiaire étudié (7). Ray et coll. observent une stabilité d’au moins 100 minutes, avec un raccourcissement relatif non significatif d’environ 3 % par rapport à 30 minutes (8). Toulon et coll. suggèrent une stabilité comprise entre 1 et 2 heures, sans toutefois démontrer formellement celle à 2 heures, puisque 23,6 % des résultats (29/123) sont discordants à 4 heures (10). Bien que la majorité de ces discordances se situe à proximité des limites inférieure et supérieure de l’intervalle thérapeutique, elles auraient néanmoins conduit à une modification de la prise en charge du traitement anticoagulant chez 10 patients sur 123 (8 %). Billoir et coll. rapportent une stabilité du TCA jusqu’à 4 heures (concordance de Bland-Altman entre 1 et 4 heures : −4,0 ± 5,3 secondes) sans détailler le nombre de résultats discordants (9). Plus récemment, Gremillet et coll. concluent à une stabilité jusqu’à 6 heures, mais les coefficients Kappa entre 1 heure et 6 heures (0,64 et 0,79 selon les réactifs) indiquent un nombre significatif de résultats discordants, dont l’impact clinique n’a pas été rapporté (11).
Pour l’activité anti-Xa, Ray et coll. rapportent une stabilité de 100 minutes en sang total, sans étude au-delà (8), Billoir et coll. et Toulon et coll. indiquent une stabilité jusqu’à 4 heures, et Gremillet et coll. jusqu’à 6 heures (9-11). Dans l’étude de Billoir et coll., la concordance entre 1 heure et 4 heures est excellente (1,10 × 10−⁹ ± 0,058 UI/mL), bien que 5 échantillons sur 31 (16 %) présentent un biais de plus de 15 % (3 plus élevés : 200 %, 125 %, 119 % ; 2 plus faibles : 84 %, 83 %), sans impact clinique (9). Toulon et coll. montrent qu’un temps de 1 à 4 heures entraîne un reclassement non négligeable des patients, avec 9 % passant de la zone thérapeutique à sous-thérapeutique et < 1 % de suprathérapeutique à thérapeutique (10). Enfin, Gremillet et coll. rapportent des coefficients Kappa entre 1 heure et 6 heures de 0,73 et 0,8 selon les réactifs anti-Xa, indiquant là encore un nombre significatif de résultats discordants (11).
Durées maximales en plasma (de la centrifugation à l’analyse) selon les auteurs
Si le prélèvement sur tube citrate est centrifugé rapidement, au plus tard dans l’heure suivant le prélèvement, Heil et coll. ont montré que le TCA reste stable pendant 24 heures lorsque le plasma est conservé à 6 °C et moins de 8 heures si le plasma est conservé à température ambiante (réduction du TCA de 13 % à 8 heures pour une limite acceptable définie arbitrairement à 10 %) (6). Toulon et coll. concluent à une stabilité inférieure à 4 heures et Gremillet et coll. estiment quant à eux la stabilité du TCA à 6 heures pour le plasma citraté décanté et analysé avec le réactif STA PTT-A de Stago, et de moins de 4 heures avec le réactif Actin FS de Siemens (11). Toutefois, dans le premier cas, le coefficient Kappa entre 1 heure et 6 heures était de 0,70 et dans le second, entre 1 heure et 4 heures, de 0,51. L’absence de mise à disposition des données individuelles de cette étude ne permet pas d’évaluer l’impact clinique de ces discordances.
Concernant la stabilité de l’activité anti-Xa mesurée sur plasma citraté, Toulon et coll. indiquent que la stabilité est inférieure à 4 heures à température ambiante avec deux réactifs différents contenant tous les deux du sulfate de dextran. En effet, avec cette durée, 8 résultats sur 62 (12,9 %) étaient discordants, la plupart à la limite inférieure de l’intervalle thérapeutique donc sans impact sur le management du traitement par HNF (10). Gremillet et coll. concluent eux à une stabilité de 6 heures, que le réactif utilisé contienne ou non du sulfate de dextran (11). Le coefficient Kappa entre 1 heure et 6 heures était de 0,76 pour le réactif Siemens contenant du sulfate de dextran, et de 0,67 pour le réactif Stago sans sulfate de dextran, soulignant la présence de données discordantes.
DISCUSSION
Cette revue met en évidence une variabilité importante des résultats concernant la stabilité du TCA et de l’activité anti-Xa dans le suivi de l’HNF à dose thérapeutique. Toutefois, le nombre d’études disponibles reste limité, avec seulement neuf études identifiées sur une période de près de 40 ans, dont une seule étude prospective. Ce faible nombre d’études, associé à leur hétérogénéité méthodologique, limite la robustesse des conclusions et la possibilité d’établir des recommandations fondées sur des preuves solides. Néanmoins, les données disponibles confirment que la phase préanalytique constitue un déterminant majeur de la fiabilité du suivi biologique des patients sous HNF.
Un constat global de cette analyse est qu’aucune des études publiées ne satisfait l’ensemble des critères de la checklist CRESS, développée par le groupe de travail préanalytique de l’EFLM afin d’harmoniser la conception et la publication des études de stabilité et publiée en 2020 (2). Toutefois, ce constat doit être nuancé, dans la mesure où la quasi-totalité des neuf études ont été publiées avant 2020, à l’exception de celle de Gremillet et coll. (11), et n’ont donc pas pu intégrer les critères CRESS lors de leur conception. Bien que certains paramètres techniques, tels que les méthodes analytiques, soient généralement décrites, des informations essentielles peuvent être manquantes. Ainsi, l’indication du traitement par HNF des patients prélevés, le nombre d’échantillons par patient, les caractéristiques des patients, les modalités de transport et les conditions de température sont rarement précisés. De plus, les données individuelles sont rarement disponibles, ce qui empêche d’évaluer précisément l’impact clinique des variations observées.
Une lacune méthodologique majeure concerne également les critères d’acceptabilité utilisés pour définir la stabilité. Ceux-ci sont rarement précisés et, lorsqu’ils le sont, reposent le plus souvent sur des critères statistiques arbitraires, sans justification fondée sur leur pertinence clinique. Très peu d’études ont évalué l’impact des variations observées sur le reclassement thérapeutique des patients, alors que ce paramètre constitue l’élément le plus pertinent en pratique clinique. Cette absence de critères d’acceptabilité cliniquement validés, associée au non-respect des critères CRESS et au nombre limité d’études disponibles, limite la validité des conclusions. Par ailleurs, à notre connaissance, aucune étude de stabilité conforme à ces critères n’a, à ce jour, été publiée dans le domaine de l’hémostase en général, et leur application est tout juste émergente dans les autres domaines de la médecine de laboratoire. L’objectif de ces recommandations n’est pas de remettre en cause les travaux antérieurs, mais de renforcer le niveau de confiance dans les résultats des études futures. Les recommandations du Clinical and Laboratory Standards Institute (CLSI) préconisent une centrifugation dans l’heure suivant le prélèvement pour le TCA et dans les 4 heures pour l’activité anti-Xa, ainsi qu’une analyse dans les 4 heures si le plasma est rapidement séparé des cellules sanguines (15). La Société française de thrombose et d’hémostase (SFTH) recommande pour le TCA et l’activité anti-Xa une centrifugation dans les 2 heures pour le sang total conservé à température ambiante et une analyse du plasma dans les 4 heures suivant le prélèvement, sous réserve d’une centrifugation réalisée dans l’heure, et une durée acceptable de 5 heures en sang total ou en plasma pour les prélèvements sur tubes CTAD (16). Néanmoins, ces recommandations reposent sur un niveau de preuves limité. Notre revue de la littérature montre qu’en sang total, la stabilité du TCA et de l’activité anti-Xa n’est pas suffisamment documentée à partir de la durée de référence la plus courte, à savoir d’une heure après le prélèvement. Au-delà de cette durée, la libération progressive du FP4 peut entraîner une sous-estimation de l’activité anticoagulante et conduire à un reclassement thérapeutique inapproprié. Les données disponibles suggèrent que l’estimation du niveau d’héparine par test d’activité anti-Xa présente une stabilité légèrement supérieure à celle du TCA en sang total. Toutefois, à 4 heures, des discordances susceptibles d’avoir un impact clinique sont observées pour environ 10 % des échantillons que ce soit pour le TCA ou l’activité anti-Xa, tandis que les données à 2 heures restent très limitées. Après centrifugation, la stabilité apparaît améliorée, mais les données disponibles restent limitées et ne permettent pas d’estimer l’éventuel impact clinique de l’allongement des durées. Une analyse rapide après centrifugation semble constituer un objectif valable, qui ne tient qu’à l’organisation du laboratoire, avec une durée, sans décantation, ne dépassant pas 10 minutes afin de minimiser le risque de variations préanalytiques. L’utilisation de tubes CTAD, conçus pour limiter l’activation plaquettaire et la libération du FP4, réduirait la neutralisation in vitro de l’héparine. Toutefois, les études disponibles rapportent des durées de stabilité globalement similaires à celles observées avec les tubes citrate, sans bénéfice clinique clairement établi. Par ailleurs, leur utilisation courante demeure limitée en raison de leur coût plus élevé (2 à 4 fois supérieur à celui des tubes citrate), de leur disponibilité restreinte et de leur sensibilité à la lumière. De même, la présence de sulfate de dextran dans certains réactifs d’anti-Xa, susceptible de favoriser la dissociation de l’héparine du FP4, ne semble pas améliorer significativement la stabilité des résultats, bien que les données disponibles soient limitées et ne permettent pas de conclusions définitives. De plus, juste après l’administration de protamine pour neutraliser l’HNF, le niveau en activité anti-Xa évalué avec un réactif contenant du sulfate de dextran est surestimé (12,13).
En conclusion, le nombre limité d’études disponibles, leur hétérogénéité méthodologique, le non-respect des critères CRESS et l’absence de critères d’acceptabilité cliniquement validés clairs et consensuels ne permettent pas d’établir des recommandations fondées sur des preuves robustes. Une approche prudente consiste à mettre en oeuvre les moyens permettant une centrifugation dans l’heure suivant le prélèvement et une analyse aussi rapide que possible après centrifugation. Des études prospectives, méthodologiquement rigoureuses et conformes aux récents critères CRESS, incluant des effectifs suffisants et des critères cliniquement pertinents, sont nécessaires pour déterminer si des durées préanalytiques plus longues et moins contraignantes peuvent être envisagées sans compromettre la fiabilité des résultats ni la pertinence des décisions thérapeutiques, tout en garantissant la transmission des résultats dans des durées compatibles avec les besoins cliniques, donc aussi courtes que possible. Ces données sont essentielles pour établir des recommandations fiables et garantir une prise en charge sécurisée des patients traités par HNF à dose thérapeutique.
POINTS CLÉS À RETENIR
• La phase préanalytique constitue un déterminant majeur de la fiabilité des mesures du TCA et de l’activité anti-Xa chez les patients traités par HNF.
• Un allongement de la durée écoulée entre le prélèvement, la centrifugation et l’analyse peut entraîner une sous-estimation de l’activité anticoagulante, liée notamment à la neutralisation in vitro de l’héparine par le facteur plaquettaire 4.
• Les données disponibles ne soutiennent pas suffisamment des temps plus longs qu’une centrifugation au mieux dans l’heure suivant le prélèvement, et une analyse précoce (10 minutes, sans décantation).
• En conséquence, une approche prudente consiste à mettre en oeuvre les moyens permettant de respecter ces durées.
• Le nombre limité d’études disponibles et leur hétérogénéité méthodologique soulignent la nécessité d’études prospectives rigoureuses, conformes aux critères CRESS, afin d’établir des recommandations préanalytiques fondées sur des données probantes, correspondant aux profils contemporains de malades anticoagulés avec de l’HNF, qui pourraient permettre une extension à deux heures.
Liens d’intérêts : les auteurs déclarent ne pas avoir de lien d’intérêt en rapport avec cet article.