ÉDITION SPÉCIALE EAHAD 2026
19th Annual Congress of the European Association for Haemophilia and Allied Disorders
Du 3 au 6 février 2026, Dublin
Avec le soutien institutionnel
![]()
![]()
D’après la communication orale de Marti Olivieri (on behalf of the PedNet study group), Update on inhibitor development for individual FVIII concentrates in PUPs with severe haemophilia A in the PedNet registry. 19th Annual Congress of the European Association of Haemophilia and Allied Disorders 2026, 3-61 February.
Birgit Frotscher, Nancy
Le développement d’un inhibiteur anti-FVIII reste l’une des complications redoutées chez les enfants atteints d’hémophilie A sévère, avec environ 96 % des inhibiteurs survenant au cours des 50 premiers jours d’exposition (ED) au FVIII.
Cette étude analyse l’incidence des inhibiteurs en fonction du concentré de FVIII chez 1 503 patients précédemment non traités (PUPs) atteints d’hémophilie A sévère, nés entre 2000 et 2024, issus de la cohorte PedNet. Les patients ont été suivis jusqu’au développement d’un inhibiteur ou jusqu’à 50 ED. Les analyses ont été ajustées sur les principaux facteurs de risque connus.
Au total, 444 patients ont développé un inhibiteur. Aucune différence significative de risque n’a été observée entre les concentrés plasmatiques et recombinants (30 % vs 31 %), ni entre les concentrés recombinants à demi-vie standard et ceux à demi-vie prolongée (30 %). L’analyse selon chaque marque de concentré, utilisant l’octocog alfa (Advate®) comme référence, met en évidence un risque plus élevé avec l’octocog alfa (Kogenate®) et le concentré de FVIII contenant la protéine von Willebrand (Fanhdi®), tandis que le turoctocog alfa est associé à un risque plus faible, mais le nombre de patients exposés reste assez faible (n = 40) (Figure 1).
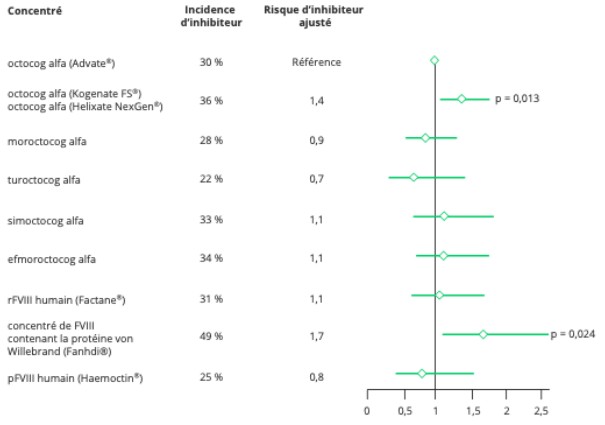
Figure 1 : Comparaison du risque d’inhibiteur des différents concentrés en FVIII
Cette étude, la plus vaste menée à ce jour chez les PUPs, confirme un risque global d’inhibiteur d’environ 31 % au cours des 50 premiers ED, mais ne met pas en évidence de différence majeure entre les classes de concentrés de FVIII, tout en soulignant des variations de risque pour certains produits spécifiques. Toutefois, l’hétérogénéité importante des pratiques thérapeutiques entre les pays, de stratégies en termes de traitement initial et d’accès aux différentes options thérapeutiques, pourrait influencer les comparaisons observées. Les hypothèses pouvant expliquer que des études antérieures ont retrouvé un risque d’inhibiteur chez les PUPs significativement plus faible avec les FVIII plasmatiques par rapport aux FVIII recombinants ne sont pas discutées.

