ÉDITION SPÉCIALE EAHAD 2026
19th Annual Congress of the European Association for Haemophilia and Allied Disorders
Du 3 au 6 février 2026, Dublin
Avec le soutien institutionnel
![]()
![]()
D’après la présentation orale de Hermans C. Factor IX replacement-appraising the options.
19th Annual Congress of the European Association of Haemophilia and Allied Disorders 2026 3-6 February
Hortense Maynadié, le Kremlin-Bicêtre
La capacité du facteur IX (FIX) à se lier de façon réversible au collagène IV (ColIV) conditionne sa biodistribution entre compartiment intravasculaire, mesurable, et extravasculaire, non accessible aux dosages usuels, mais participant pleinement à l’hémostase. Après passage du plasma vers le sous-endothélium, voire plus profondément dans la paroi vasculaire, le FIX peut être relargué dans la circulation. Ce pool tissulaire, situé à proximité du complexe FVIIa–facteur tissulaire, contribue en partie à l’hémostase et une altération de la liaison du FIX au ColIV est associée à une tendance hémorragique majorée chez les souri (Figure 1).
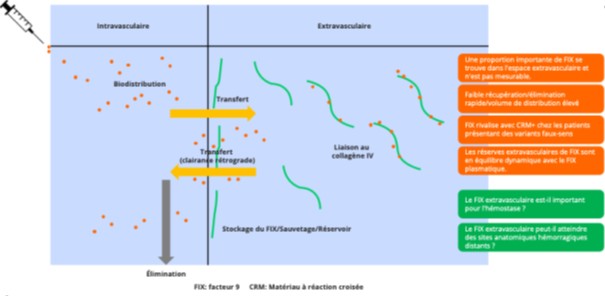
Figure 1 : Biodistribution du FIX
Cette biodistribution spécifique du FIX a des implications sur le choix du type de FIX à prescrire en fonction des patients et des circonstances cliniques. En chirurgie, la disponibilité immédiate du FIX intravasculaire est essentielle alors qu’en prophylaxie, la constitution et la saturation du compartiment extravasculaire apparaissent au moins aussi importantes. Par ailleurs, chez les patients hémophiles B sévères CRM+, le FIX endogène dysfonctionnel entre en compétition avec le FIX administré, et certains modèles suggèrent que leurs besoins sont plus élevés que chez les sujets CRM− pour atteindre une protection équivalente (Figure 2).
Ces éléments de pharmacocinétiques sont également essentiels pour interpréter les différences pharmacocinétiques entre les différents FIX à demi-vie prolongée (EHL). Si le FIX, qu’il soit fusionné au fragment Fc d’une IgG (rIX-Fc), à l’albumine (rIX-FP) ou pégylé (N9-GP) affiche une efficacité clinique globalement comparable, les taux résiduels plasmatiques différents, sans corrélation avec le phénotype hémorragique. Or, les modifications du FIX influencent sa biodistribution et sa liaison au ColIV. Le FIX-Fc diffuse davantage en extravasculaire et ne modifie pas l’affinité du FIX natif pour le ColIV, ce qui se traduit par un volume de distribution supérieur (300 ml/kg vs 100ml/kg pour le FIX-FP et 50ml/kg pour le N9-GP) ; ainsi, des saignements rapportés sous FIX-FP malgré des taux plasmatiques élevés interrogent sur la signification clinique des taux résiduels (Figure 2).
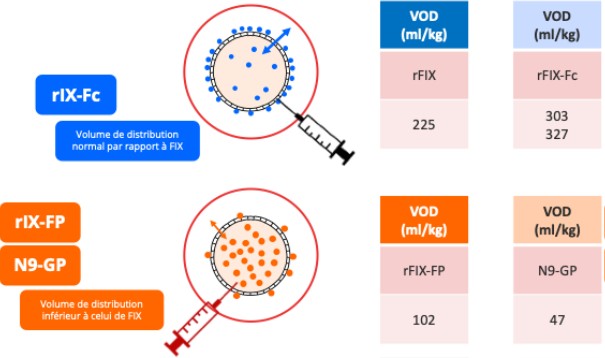
Figure 2 : Différents potentiels de distribution extravasculaire des EHL-FIX
De la même façon, après qu’un patient ait reçu une thérapie génique, la contribution du FIX-Padua extravasculaire à l’hémostase reste à élucider, afin de choisir le type et la dose nécessaire de FIX pour une chirurgie par exemple.
Alors, quel serait le FIX idéal du futur ? L’étude de Kristin Hovden Aaen et al. a exploré comment des mutations diminuant ou renforçant la liaison au ColIV modulent la distribution, la demi-vie et l’efficacité hémostatique d’un FIX-Padua fusionné à l’albumine. Chez des souris avec une hémophilie B, l’augmentation de l’affinité de ce FIX hyperactif pour le colIV entraine une distribution extravasculaire accrue et une demi-vie fonctionnelle nettement prolongée (environ 80 h) 2. Ces résultats indiquent que l’ingénierie ciblée de la liaison au collagène peut encore prolonger l’efficacité du FIX, ouvrant la voie à des stratégies thérapeutiques nouvelles pour l’hémophilie B.

