ÉDITION SPÉCIALE EAHAD 2026
19th Annual Congress of the European Association for Haemophilia and Allied Disorders
Du 3 au 6 février 2026, Dublin
Avec le soutien institutionnel
![]()
![]()
D’après les communications orales de :
- Wolfgang Miesbach, University Hospital of Frankfort, Germany
- Thierry Vandendriesche, Vrije Universitet Brussels, Belgium
Current and future gene therapy approaches for bleeding disorders; Capturing outcomes and managing gene therapy. 19th Annual Congress of the European Association of Haemophilia and Allied Disorders 2026,3-6 February.
Antoine Babuty, Nantes & Birgit Frotscher, Nancy
Les 2 présentations ont fait le point sur la thérapie génique (TG) dans l’hémophilie A et B, après plus de dix années d’expérience clinique. À ce jour, deux thérapies géniques ont été approuvées pour l’hémophilie B et une pour l’hémophilie A, toutes reposant sur l’utilisation de vecteurs adéno-associés (AAV). Les données issues des essais de phase III et du suivi à long terme confirment une efficacité clinique durable, particulièrement marquée dans l’hémophilie B.
La thérapie génique de l’hémophilie B est un traitement qui a reçu en France une autorisation de commercialisation dans l’hémophilie B (HB) sévère et modérément sévère. Elle consiste en l’injection d’un vecteur AAV5 comprenant un transgène du facteur IX (FIX).
L’injection de 50*1012gc/kg (n = 3 participants) ou de 2*1013 gc/kg (n = 5 participants) permet la persistance de la production de facteur IX dans les 2 cohortes à des taux stables à 9 ans : médiane (range) 5,0 UI/dL (3,2-5,5) et 5,7 IU/dL (2,9-7,0) respectivement (Figure 1).
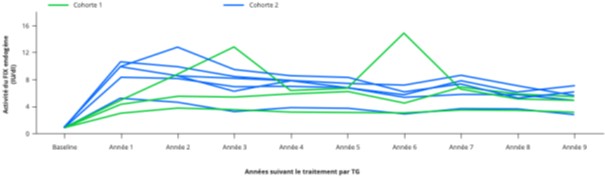
Figure 1 : Évolution des taux de facteur IX neuf ans après l’injection de thérapie génique
Cela se traduit par une réduction soutenue des saignements, traités ou non (Figure 2), ainsi que par la diminution de la consommation en FIX. Aucun des participants n’a repris de prophylaxie par FIX. Aucun évènement indésirable grave n’a été rapporté (absence de développement d’inhibiteur, d’évènement thromboembolique, de toxicité hépatique ou de cancer lié à l’AAV).
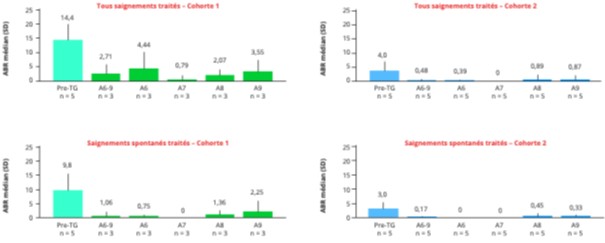
Figure 2 : Saignements annualisés médians chez les patients ayant reçu une injection de thérapie génique
La thérapie génique dans l’hémophilie B ayant reçu les autorisations de mise sur le marché correspond au même vecteur et transgène, hormis la substitution de deux nucléotides permettant la synthèse du FIX Padua, qui est une protéine hyperactive. A la posologie préconisée de 2*1013 gc/kg, les résultats à 5 ans dans l’étude HOPE-B montrent également une persistance des taux de FIX à des taux plus élevés. Il est fortement probable que ces taux se maintiennent également dans le temps. La thérapie génique apparaît donc comme un traitement efficace et sûr à long terme pour le traitement de l’hémophilie B sévère et modérément sévère.
Dans l’hémophilie A, la situation est un peu différente. Après la thérapie génique, le taux de facteur VIII (FVIII) augmente d’abord initialement jusqu’à des valeurs quasi normales, puis diminue progressivement pour se stabiliser autour de 15 à 20 % après 3 à 5 ans (Figure 3). Malgré cette baisse, le traitement reste efficace sur le plan clinique chez la majorité des patients. Cependant, une variabilité interindividuelle de réponse importante est observée, tant en ce qui concerne le niveau d’expression initiale que sa durabilité.
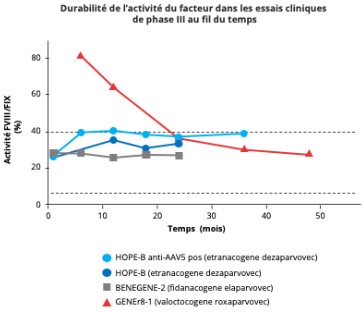
Figure 3 : Expression à long terme du FVIII/FIX dans les études de phase III
Concernant l’immunogénicité, trois patients atteints d’une hémophilie A traités par TG ont développé un inhibiteur : pour l’un deux, un an environ après la TG, et pour les deux autres, dans le cadre d’un essai évaluant un FVIII-ET3 contenant une séquence porcine. Dans une autre étude incluant des patients ayant déjà eu un inhibiteur, aucun des sept patients dont l’inhibiteur avait disparu n’a présenté de récidive. En revanche, parmi trois patients ayant encore un inhibiteur actif, une recirculation de FVIII après la TG n’a été objectivée que dans un cas.
Les causes permettant de comprendre les différences de résultats observés entre les patients après TG et la diminution de l’expression du gène FVIII ne sont pas encore totalement connues, mais plusieurs hypothèses ont été soulignées (Figure 4). Les biopsies hépatiques réalisées montrent qu’il pourrait exister des variations relatives aux mécanismes d’activation et de régulation du gène, ainsi qu’un rôle possible de certaines protéines cellulaires (protéines chaperonnes) et d’une réaction immunitaire impliquant les lymphocytes T. Les modèles murins indiquent, pour le FVIII, qu’une production trop importante du transgène pourrait provoquer un stress des cellules hépatiques (non spécialisées pour fabriquer cette protéine) ce qui entraînerait une perte progressive d’expression du transgène.
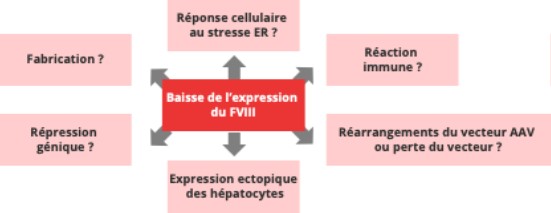
Figure 4 : Hypothèses des causes de la diminution de l’expression du FVIII
Enfin, de nouvelles stratégies sont en cours de développement pour améliorer ces thérapies géniques. Elles pourraient impliquer l’utilisation de variants dont l’activité et/ou la demi-vie d’élimination sont accrues (FIX triple mutant, FIX-Padua fusion-albumine, FVIII-QQ résistant à l’APC). À plus long terme, l’usage de méthodes reposant sur les techniques d’édition du génome, comme CRISPR-Cas9, pourraient permettre d’intégrer le gène directement dans l’ADN de façon plus stable, même si des questions de sécurité restent à résoudre.
En conclusion, la thérapie génique commence à être utilisée en pratique clinique dans l’hémophilie. Son effet est durable et solide pour le FIX, mais moins stable pour le FVIII. Il reste encore à mieux comprendre la variabilité de l’expression inter-individuelle du transgène et pourquoi l’expression du FVIII diminue avec le temps, afin de développer de nouvelles thérapies plus régulières dans leurs résultats, plus durables et plus prévisibles.

