Les eryghosts, un nouvel acteur de la thrombose dans les anémies hémolytiques ?
INTRODUCTION
En 2014, Arraud et coll. ont caractérisé les vésicules extracellulaires retrouvées dans le plasma de volontaires sains. Ces travaux ont conduit à la découverte de vésicules érythroïdes de grande taille (6-8μm), exposant massivement la phosphatidylsérine, présentes en très faible quantité dans le plasma. Ces vésicules présentent une taille similaire à celle des globules rouges (GR), mais leur complexité interne est très différente de ces derniers, en lien avec la perte d’une grande partie de l’hémoglobine intracellulaire. Le même type de vésicule peut être généré in vitro en provoquant l’hémolyse de GR. Ces caractéristiques ont conduit à leur dénomination de « fantômes » de globule rouge, ou eryghosts (1).
ORIGINE PHYSIOLOGIQUE DES ERYGHOSTS : L’HÉMOLYSE INTRA-SPLÉNIQUE
En 2020, Klei et coll. ont décrypté l’origine de la formation des eryghosts in vivo lors de la clairance physiologique des GR sénescents. Leurs travaux ont montré la présence, dans les macrophages de la pulpe rouge splénique, de vésicules de la taille d’un globule rouge, mais largement dépourvues d’hémoglobine, correspondant à la description des eryghosts. Dans un modèle murin, ils ont transfusé des GR sénescents marqués avec un traceur intra-cellulaire et un traceur membranaire et ont observé que les GR sénescents sont retenus dans la rate et perdent leur marquage intracellulaire, indiquant une hémolyse, avant leur phagocytose par les macrophages. En physiologie, les eryghosts seraient donc formés à partir des GR sénescents par un processus d’hémolyse intrasplénique. Le signal suspecté d’être à l’origine de l’hémolyse des GR sénescents en eryghosts est l’exposition de la protéine Lu/BCAM, et son interaction avec la laminine endothéliale splénique (2). Les auteurs ont par ailleurs montré in vitro que les eryghosts sont phagocytés par les macrophages de la pulpe rouge splénique, contrairement aux GR sénescents, sans toutefois décrire le mécanisme impliqué dans cette reconnaissance (2).
LA PROTÉINE S : UN ACTEUR CLÉ DE L’ÉLIMINATION SPLÉNIQUE DES ERYGHOSTS
La protéine S est surtout connue comme protéine anticoagulante majeure, en étant le cofacteur de la protéine C activée et du TFPI (tissue factor pathway inhibitor). Néanmoins, cette protéine est également impliquée dans le processus d’élimination physiologique des cellules apoptotiques exposant de la phosphatidylsérine. La protéine S forme un pont moléculaire en se liant d’une part à la phosphatidylsérine exposée par les cellules apoptotiques via son domaine Gla, et d’autre part au récepteur MerTK exprimé par les macrophages via son domaine SHBG (sex hormon binding globulin). Comme pour les cellules apoptotiques, la protéine S promeut la phagocytose des eryghosts (exposant massivement la phosphatidylsérine) par les macrophages exprimant MerTK (3). La découverte de ce nouveau mécanisme permet de mieux comprendre les mécanismes de clairance physiologique des GR mais pourrait également avoir des implications physiopathologiques.
LES ERYGHOSTS CIRCULANTS : IMPLICATION DANS LA PHYSIOPATHOLOGIE DE LA DRÉPANOCYTOSE
Les données actuelles sur la pathogénicité des eryghosts ont été majoritairement rapportées dans le cadre de la drépanocytose. Cette pathologie est liée à une mutation ponctuelle sur le gène de la β-globine humaine, conduisant à la synthèse d’une hémoglobine anormale, l’hémoglobine S. Trois processus sont au coeur de la physiopathologie de la drépanocytose : la polymérisation de l’hémoglobine S, l’hémolyse, et la vaso-occlusion. Chez ces patients, une activation chronique de la coagulation est observée, qui à son tour favorise la vaso-occlusion, entraînant un cercle vicieux (4).
Des travaux ont rapporté la présence de vésicules avec les mêmes caractéristiques que les eryghosts dans le sang total de patients drépanocytaires, où elles sont retrouvées en bien plus grande quantité que chez les volontaires sains (5,6). L’origine de l’accumulation des eryghosts chez les patients drépanocytaires est multiple. La quantité d’eryghosts circulants est corrélée à l’intensité de l’hémolyse observée chez les patients (réticulocytes, lactate déshydrogénase et bilirubine), mais aussi à la sévérité de l’atteinte de leur fonction splénique. Chez ces patients, une diminution modérée des taux de protéine S est également fréquemment retrouvée. Dans une cohorte française de 45 patients, les patients avec les taux les plus élevés d’eryghosts
présentaient des taux de protéine S significativement diminués (3).
L’extraction des eryghosts à partir du plasma de patients avec une drépanocytose a permis d’évaluer leur pathogénicité. L’ajout de concentrations croissantes d’eryghosts isolés a entraîné une augmentation significative de la génération de thrombine et de fibrine mesurées dans un plasma normal, un effet possiblement lié à l’exposition massive de phosphatidylsérine à leur surface (3). Ces résultats sont corroborés par d’autres travaux ayant mis en évidence un allongement du temps de coagulation du plasma des patients drépanocytaires testés lorsque ces vésicules en sont extraites (6). Par ailleurs, les eryghosts ont montré in vitro une adhérence accrue à un endothélium activé par rapport à des GR intacts de patients drépanocytaires. Cette caractéristique est particulièrement importante dans le cadre de la drépanocytose, car la vaso-occlusion de la microvasculature par des agrégats de cellules adhérant à l’endothélium est un élément physiopathologique majeur (3).
Dans le contexte de la drépanocytose, il est probable que l’hémolyse intravasculaire pathologique entraîne la formation d’eryghosts dans la circulation. Ce phénomène pourrait dépasser les capacités d’élimination de la rate, surtout dans un contexte d’hyposplénisme et de diminution des taux de protéine S associés à la maladie. Les eryghosts s’accumulent alors dans le sang périphérique, entraînant un cercle vicieux en favorisant l’activation de la coagulation, la consommation de la protéine S, et l’adhérence aux cellules endothéliales (Figure 1).
ERYGHOSTS ET THROMBOSE : AU-DELÀ DE LA DRÉPANOCYTOSE
Au-delà de la drépanocytose, d’autres pathologies liées au GR sont associées à des complications thrombotiques. C’est le cas notamment d’anémies hémolytiques telles que l’hémoglobinurie paroxystique nocturne et l’anémie hémolytique auto-immune à anticorps chauds (7). La physiopathologie de ces événements thrombotiques associés aux hémolyses n’est pas complètement élucidée. Ces complications sont également particulièrement fréquentes chez les patients atteints de polyglobulie de Vaquez, chez qui les érythrocytes présentent une adhérence augmentée à l’endothélium, médiée par l’interaction de la protéine membranaire Lu/BCAM (constitutivement phosphorylée du fait de la présence de JAK2V617F) avec la laminine endothéliale (8). Cette même interaction étant à l’origine de la formation des eryghosts (2), et à la lumière des données disponibles sur les propriétés procoagulantes des eryghosts, ces derniers pourraient jouer un rôle dans les complications thrombotiques associées à ces pathologies. Par ailleurs, la splénectomie est également associée à des complications thrombotiques, dans la période postopératoire immédiate, mais de façon intéressante, ce risque persiste particulièrement chez les patients présentant toujours une hémolyse chronique (drépanocytose, thalassémie intermédiaire, anémie hémolytique autoimmune) après la splénectomie (9). L’étude des taux de protéine S et de la concentration d’eryghosts dans le sang périphérique dans ces différentes pathologies serait particulièrement intéressante pour continuer à étudier le rôle physiopathologique des eryghosts et de leur propriétés procoagulantes.
Dans le contexte de la COVID-19, un nouveau mécanisme de dépôt de membranes de GR hémolysés aux sites de la nécroptose de cellules endothéliales aboutissant à un mécanisme hémostatique a été décrit. Ce phénomène ne conduisait pas à la formation d’agrégats plaquettaires ou de fibrine mais à l’agrégation des GR et l’obstruction microvasculaire, puis à des lésions ischémiques d’organe (10). La question de la nature exacte de ces membranes de GR hémolysés, et de leur lien avec les eryghosts reste ouverte. Cette question met en lumière le manque actuel de caractérisation précise des eryghosts, population encore peu décrite dans la littérature et souvent sous des dénominations différentes, bien qu’avec des caractéristiques identiques (taille, nature érythroïde, perte du contenu intracellulaire, exposition de la phosphatidylsérine).
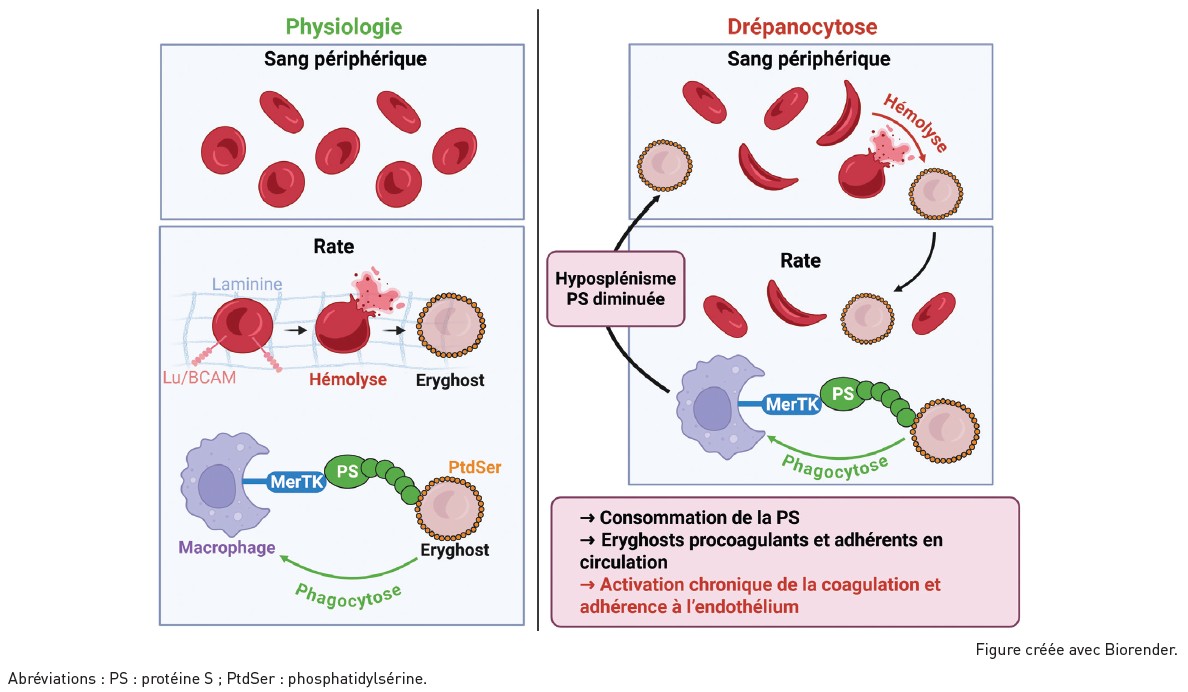
Figure 1 : Les eryghosts en physiologie et dans le contexte de la drépanocytose.
Figure 1: Eryghosts in physiology and in the context of sickle cell disease.
POINTS CLÉS À RETENIR
• Les eryghosts sont des vésicules issues de l’hémolyse des globules rouges exposant massivement la phosphatidylsérine.
• Les eryghosts sont produits physiologiquement dans la rate, où ils sont éliminés par les macrophages. La protéine S favorise leur reconnaissance et leur élimination.
• L’accumulation des eryghosts dans le sang périphérique a été observée dans la drépanocytose, en rapport avec une hémolyse accrue et un défaut de clairance.
• Les eryghosts ont des propriétés procoagulantes et adhèrent à un endothélium activé, pouvant contribuer aux complications vasculaires de la drépanocytose mais également à d’autres pathologies hémolytiques.
Liens d’intérêts : les auteurs déclarent ne pas avoir de lien d’intérêt en rapport avec cet article.

