RÉSUMÉ
Bien que présents en grande quantité dans les caillots sanguins, les globules rouges ont longtemps été considérés comme des acteurs passifs de la coagulation. Aujourd’hui, il est reconnu qu’ils jouent un rôle actif dans l’hémostase et la thrombose. Ainsi, des anomalies de l’hématocrite, de la déformabilité ou de l’agrégation érythrocytaire influencent l’hémostase directement ou via leur impact sur la viscosité sanguine. La sénescence érythrocytaire, qui s’accompagne de modifications membranaires telles que l’externalisation de la phosphatidylsérine, l’expression accrue de molécules d’adhérence et l’émission de microparticules, module également la coagulation. Ces changements peuvent affecter l’adhérence des globules rouges à la paroi vasculaire, la réactivité et la margination plaquettaire, la structure de la fibrine et la sensibilité à la fibrinolyse, notamment par la formation de polyhédrocytes lors de la contraction des caillots. Les observations cliniques liant phénotype érythrocytaire et anomalies de coagulation soulignent le potentiel des globules rouges comme cible thérapeutique dans les dysfonctionnements hémostatiques et les pathologies thrombotiques.MOTS CLÉS
caillots sanguins, coagulation, érythrocytes, rhéologie
ABSTRACT
Although very abundant in thrombi, red blood cells (RBCs) have long been considered as passive players in coagulation. Recent evidence highlights their active role in hemostasis and thrombosis. Quantitative or qualitative alterations of RBCs can disrupt coagulation: hematocrit, RBC deformability, and aggregation influence hemostasis directly or via their effects on blood viscosity, which impact on blood flow velocity and structure. RBC senescence is characterized by membrane changes, including phosphatidylserine exposure, increased adhesion molecules expression, and microparticles release, which may impact on coagulation. These changes affect RBCs adhesion to the vessel wall, platelet reactivity and margination, fibrin structure, and fibrinolytic sensitivity, notably through polyhedral RBCs formation during clot contraction. Clinical associations between RBC phenotype and coagulation abnormalities underscore RBCs as potential therapeutic targets in hemostatic and thrombotic disorders.
KEYWORDS
blood clots, coagulation, erythrocytes, rheology
INTRODUCTION
Les globules rouges (GRs) représentent environ 99 % des éléments figurés du sang. Longtemps considérés comme des acteurs passifs de la coagulation, leur rôle dans l’hémostase a été largement sous-estimé (1). Des données récentes montrent pourtant que les GRs participent activement à chaque étape de l’hémostase. Ainsi, des altérations quantitatives (polyglobulie, anémie) et/ou qualitatives (drépanocytose, sphérocytose) des GRs entraînent des perturbations majeures de la coagulation, favorisant des complications thrombotiques ou hémorragiques(1). Cette revue vise à explorer le rôle des GRs dans l’hémostase et les complications thrombotiques, en abordant successivement la rhéologie du sang, l’impact des propriétés rhéologiques des GRs sur l’hémostase, puis le rôle des propriétés membranaires et des motifs moléculaires associés aux dommages (DAMPs) d’origine érythrocytaire sur l’hémostase.
LA RHÉOLOGIE DU SANG
Généralités, comportement du sang
L’hémorhéologie est dédiée à l’étude des propriétés d’écoulement du sang et de ses constituants. Le sang, unique tissu liquide de l’organisme, est composé de plasma dans lequel circulent des éléments figurés, majoritairement les GRs. Leurs propriétés biophysiques, notamment de déformabilité et d’agrégation, influencent la viscosité sanguine, le flux sanguin et la fonction vasculaire (2).L’étude de l’hémodynamique peut être appréhendée à l’aide de la loi de Poiseuille : Q=(ΔP×π×r^4)/(8×η×L) , qui décrit le débit sanguin (Q) en fonction de la différence de pression(ΔP), du rayon (r) et de la longueur du vaisseau (L), ainsi que de la viscosité du sang (η). Cette loi s’applique initialement aux fluides newtoniens circulant dans des conduits rigides, ce qui n’est pas le cas du sang et de la vasomotricité vasculaire ; cependant elle reste largement utilisée dans ce contexte. Selon cette loi, toute variation de la viscosité sanguine influence directement le débit sanguin. Or, le sang n’est pas un fluide homogène et ses propriétés de viscosité dépendent des propriétés rhéologiques des GRs et des conditions hémodynamiques (3). Le sang est un fluide non newtonien, ce qui signifie que sa viscosité varie avec la vitesse de cisaillement. Il présente des propriétés rhéofluidifiantes (sa viscosité diminue lorsque la vitesse de cisaillement augmente), viscoélastiques (il existe un seuil d’écoulement en dessous duquel il ne s’écoule pas) et thixotropes (les propriétés d’écoulement varient avec le temps pour un cisaillement donné). Ces multiples propriétés soulignent la complexité de l’écoulement sanguin et la nécessité d’approches spécifiques pour en comprendre les mécanismes, les impacts potentiels sur l’environnement vasculaire et les interactions entre les différentes cellules circulantes.
La viscosité sanguine
Parmi ces propriétés rhéologiques complexes, la viscosité sanguine apparaît comme un déterminant majeur de la compréhension de l’écoulement sanguin. Elle correspond à la résistance du sang à l’écoulement et résulte des forces de friction entre ses différentes couches. Elle est définie comme le rapport entre la contrainte de cisaillement et la vitesse de cisaillement (η = τ/γ) et s’exprime en mPa·s ou en cP. De ce fait, la viscosité sanguine est élevée à faible vitesse de cisaillement, par exemple dans les veines, et diminue lorsque la vitesse de cisaillement augmente, comme dans les artères et les capillaires, traduisant le comportement rhéofluidifiant du sang (3). À faible vitesse de cisaillement, la viscosité sanguine dépend principalement de l’agrégation des GRs, tandis qu’à des vitesses élevées, elle est surtout influencée par leur déformabilité (Figure 1). L’hématocrite constitue également un déterminant majeur de la viscosité sanguine, à toutes les vitesses de cisaillement, avec un effet particulièrement marqué à faible cisaillement en raison de la formation plus importante d’agrégats érythrocytaires. La viscosité du plasma, fluide newtonien, qui dépend notamment de la concentration en protéines plasmatiques, influence également la viscosité sanguine. Enfin, bien que souvent négligée, la contribution des globules blancs peut devenir significative, en particulier dans les vaisseaux de petit diamètre ou en cas d’hyperleucocytose.
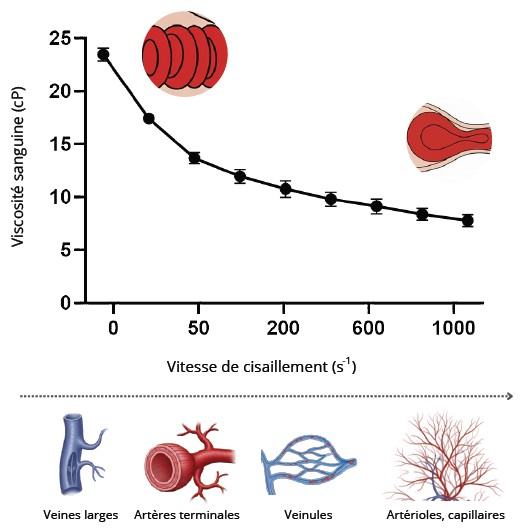
Figure 1 : Évolution de la viscosité sanguine en fonction de la vitesse de cisaillement et du territoire vasculaire considéré.
Figure 1: Changes in blood viscosity according to the shear rate and the vascular territory considered.
La viscosité sanguine diminue lorsque la vitesse de cisaillement augmente ; elle est principalement influencée par l’agrégation érythrocytaire à faible cisaillement et par la déformabilité érythrocytaire à cisaillement élevé.
L’hématocrite
Le rôle premier des GRs est d’assurer le transport de l’O2 des poumons vers les tissus, et du CO2, des tissus vers les poumons. Ce transport repose sur un rapport optimal entre la quantité de GRs et le volume sanguin, permettant d’optimiser à la fois l’apport en O2 et la perfusion tissulaire. De ce fait, une augmentation du nombre de GRs n’est pas sans conséquence. En tant que principal déterminant de la viscosité sanguine, l’hématocrite exerce une influence directe sur les propriétés d’écoulement du sang, son augmentation s’accompagnant d’une élévation marquée de la viscosité sanguine. Comme évoqué précédemment, cet effet est particulièrement prononcé à faibles vitesses de cisaillement, tandis qu’il demeure plus modéré lorsque les vitesses de cisaillement augmentent.
La déformabilité érythrocytaire
Au cours de leur vie (environ 120 jours), les GRs, biconcaves et de diamètre d’environ 7-8 μm, doivent se déformer à de multiples reprises pour traverser des capillaires très étroits, parfois même plus étroits que leur propre diamètre. Cette capacité de déformabilité, indispensable à leur fonction de transport de l’oxygène, doit être maintenue tout au long de leur vie. Cette dernière dépend de la viscosité intracellulaire, du rapport surface/volume et des propriétés viscoélastiques de la membrane, elles-mêmes influencées par l’intégrité du cytosquelette et la composition membranaire (4,5). À fort cisaillement, la membrane peut adopter un comportement de type « tank-treading », qui facilite l’alignement des GRs dans le sens du flux et réduit les résistances hémodynamiques. Une diminution de la déformabilité des GRs augmente leur fragilité, favorise l’hémolyse, complique le passage dans les capillaires fins et peut provoquer des occlusions microcirculatoires. Elle s’accompagne également d’une élévation de la viscosité sanguine, surtout dans les zones à cisaillement élevé (6).
L’agrégation érythrocytaire
Au-delà de leur capacité à se déformer, les GRs possèdent une autre propriété essentielle dans la circulation sanguine : ils peuvent se lier les uns aux autres pour former des rouleaux, ou agrégats. Deux mécanismes sont à l’origine de l’agrégation érythrocytaire :
• la théorie de la déplétion, où une zone appauvrie en macromolécules crée un gradient osmotique favorisant le rapprochement des cellules ;
• la théorie du pontage, où des macromolécules adsorbées à la surface des cellules lient les GRs entre eux (8), comme le fibrinogène par exemple.
Dans la circulation, les agrégats forment des rouleaux bi- ou tri-dimensionnels dont la dissociation nécessite une force mécanique, correspondant au « seuil de désagrégation érythrocytaire ». L’agrégation érythrocytaire est donc un phénomène réversible et favorisé à faible cisaillement, qui dépend à la fois de protéines plasmatiques comme le fibrinogène et de facteurs intrinsèques aux GRs comme le contenu membranaire en acide sialique (7). La présence de ces rouleaux dans la circulation augmente la résistance à l’écoulement et contribue ainsi à l’élévation de la viscosité sanguine, en particulier à faible cisaillement.
RÔLE DES PROPRIÉTÉS RHÉOLOGIQUES DES GLOBULES ROUGES SUR L’HÉMOSTASE
Composition physiologique des caillots sanguins
Lors de la coagulation, des interactions étroites s’instaurent entre les cellules endothéliales et les plaquettes pour favoriser la formation du caillot sanguin tout en maintenant un équilibre fragile entre les mécanismes pro et anticoagulants (9). Au coeur de ce mécanisme complexe, les interactions entre les plaquettes et les GRs, médiées par la voie FasL-FasR, jouent un rôle déterminant dans la formation du thrombus et de son devenir.
La formation du caillot étant le fruit de ces mécanismes, qui varient en fonction du territoire vasculaire, la morphologie et la composition du caillot sont dépendantes de sa localisation. En effet, la composition en fibrine, GRs, plaquettes et globules blancs est différente dans un thrombus artériel ou veineux (10). Pour un siège artériel (Figure 2A), on observe un caillot riche en fibrine et plaquettes alors que pour une localisation veineuse (Figure 2B) on observe un caillot riche en fibrine et GRs.
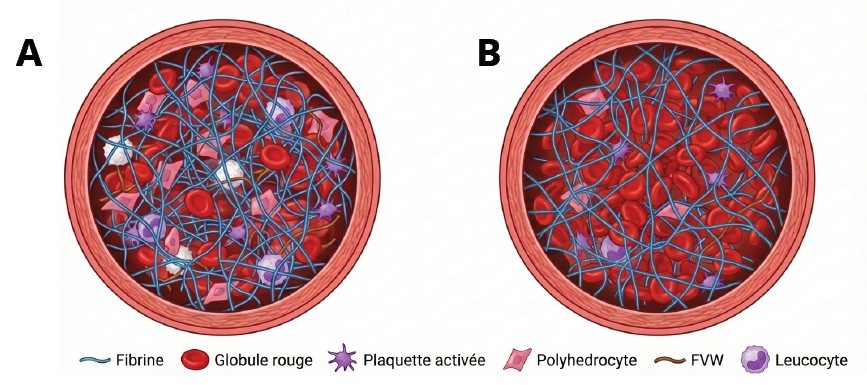
Figure 2 : Composition du caillot en fonction de sa localisation ; A) Thrombus artériel riche en plaquettes et fibrine B) Thrombus veineux riche en fibrine et globules rouges.
Figure 2: Composition of the clot depending on its location; A) Arterial thrombus rich in platelets and fibrin B) Venous thrombus rich in fibrin and red blood cells.
Impact de la rhéologie du sang sur l’hémostase et la fibrinolyse
Pour comprendre comment les modifications rhéologiques du sang influencent les différentes phases de l’hémostase, il est essentiel de se pencher sur le comportement du sang au sein de la circulation. Dans les vaisseaux dont le diamètre est inférieur à 300 μm, l’effet Fåhræus s’illustre par une diminution de l’hématocrite à mesure que le diamètre vasculaire diminue. Sous l’effet du cisaillement, les GRs déformés migrent vers l’axe du vaisseau, laissant près des parois une couche de déplétion appelée manchon plasmatique, où se concentrent plaquettes et leucocytes (Figure 3). Cette organisation favorise leur interaction avec l’endothélium et le facteur de von Willebrand (VWF). Par ailleurs, la vitesse du fluide étant réduite proche des parois, le temps de contact des cellules présentes dans le manchon plasmatique avec l’endothélium est plus élevé (11). Il est important de rappeler que la vitesse d’une particule proche de la paroi est proportionnelle à la vitesse de cisaillement et à son diamètre, et la force exercée sur une particule fixée à la paroi augmente avec la contrainte pariétale et le carré de son diamètre. Ainsi, les plaquettes (~3 μm) se déplacent plus lentement et subissent moins de force une fois adhérées que les leucocytes (~8 μm).
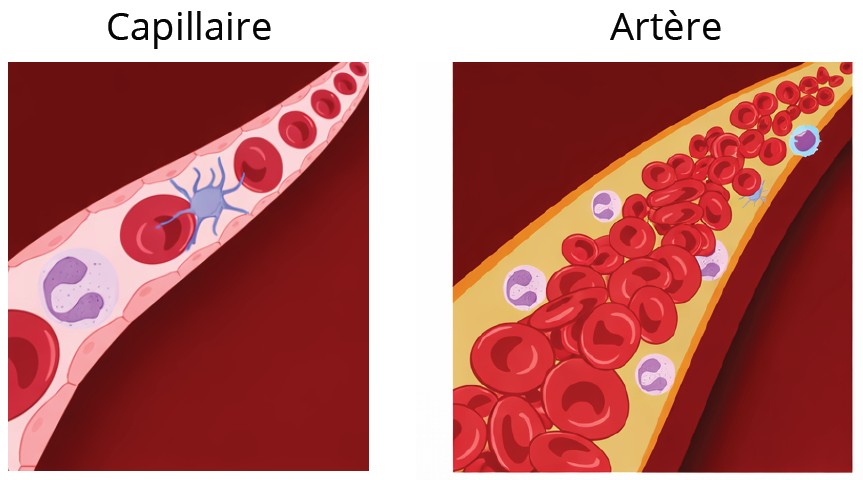
Figure 3 : Comportement de l’écoulement sanguin en fonction du territoire vasculaire.
Figure 3: Blood flow behavior depending on the vascular territory.
Dans les capillaires, les érythrocytes circulent en file indienne, et la viscosité apparente du sang est élevée. Dans les artères, la couche axiale d’érythrocytes s’épaissit tandis que le manchon plasmatique diminue, conduisant à une augmentation de la viscosité sanguine ; les thrombocytes et les leucocytes sont alors repoussés vers la périphérie du flux sanguin.
Impact de la viscosité sanguine sur les différentes phases de l’hémostase
La triade de Virchow définit trois grands facteurs favorisant la thrombose : l’atteinte de l’endothélium, l’hypercoagulabilité et la perturbation du flux sanguin. La viscosité sanguine influence ce dernier paramètre et joue donc un rôle central dans la survenue d’événements thrombotiques. Par exemple, dans les zones de faible cisaillement, une élévation de la viscosité sanguine ralentit le flux sanguin et favorise la stase. Le temps de contact prolongé entre l’endothélium et les éléments figurés, notamment les plaquettes, accroît leur probabilité d’activation. À l’inverse, dans les vaisseaux sanguins où la vitesse de cisaillement est élevée, l’élévation de la viscosité sanguine se traduit par une augmentation de la contrainte de cisaillement sur les parois vasculaires. Cette force mécanique peut entraîner le dépliement du VWF, permettant ainsi l’interaction plaquette-leucocytes et enfin l’activation plaquettaire (12).
Impact de l’hématocrite sur les différentes phases de l’hémostase
Il a été montré que des variations d’hématocrite, en s’écartant des valeurs physiologiques, s’accompagnent de perturbations de l’hémostase, les valeurs basses étant notamment associées à un retard de formation du caillot. Pour des valeurs d’hématocrite inférieures à 30 %, la contrainte de cisaillement exercée par le flux sanguin sur les parois vasculaires est insuffisante pour permettre la margination et l’adhésion des plaquettes nécessaires à l’initiation de l’hémostase primaire (13). À l’inverse, de nombreuses études ont mis en évidence une prévalence accrue d’événements thrombotiques artériels et veineux chez les patients atteints de polyglobulies (1). En effet, quelle que soit la taille des vaisseaux, l’augmentation de l’hématocrite favorise la margination des plaquettes, de façon indirecte via son impact sur la viscosité sanguine dans les plus gros vaisseaux, ou de façon directe via un effet mécanique dans les plus petits vaisseaux (< 10 μm) (3). De ce fait, in vivo, une augmentation de l’hématocrite est associée à un risque accru de survenue d’événements thrombotiques aussi bien artériels que veineux (1). Par ailleurs, il est établi qu’in vivo l’hématocrite influence la fibrinoformation de manière quantité dépendante. Ainsi, des concentrations physiologiques de GRs induisent une hétérogénéité du réseau de fibrine avec des zones plus ou moins denses en fibres (14). À l’inverse, lorsque l’hématocrite est plus élevé, le réseau est plus uniforme et les fibres plus épaisses, ce qui contribue à augmenter la stabilité mécanique du caillot (14). Paradoxalement, de récents travaux réalisés in vitro suggèrent un profil hypocoagulable mesuré par thromboélastométrie rotative chez des patients polyglobuliques, ou lorsque l’hématocrite de sujets sains est artificiellement augmenté (15). Ces données soulignent la complexité des interactions entre hématocrite et coagulation et justifient la nécessité d’études complémentaires pour mieux comprendre le rôle de l’hématocrite dans la coagulation.
Enfin, au-delà de son rôle dans l’initiation, la formation et la stabilisation du caillot, l’hématocrite apparaît également comme un déterminant majeur de sa susceptibilité à la fibrinolyse. En effet, une proportion élevée de GRs au sein du caillot modifie l’architecture du réseau de fibrine, augmentant la taille des pores entre les mailles et conférant au caillot une plus grande perméabilité aux agents lytiques, ce qui perturbe sa contraction et accélère la fibrinolyse (16). Il a d’ailleurs été démontré qu’une fraction plus élevée de GRs dans les thrombus cérébraux corrèle avec une meilleure réactivité à la thrombolyse intraveineuse. À l’inverse, une grande quantité de GRs dans le caillot peut aussi ralentir la fibrinolyse puisqu’après la contraction du caillot, les GRs constituent un joint serré et imperméable qui empêche la perfusion des agents lytiques (14).
Il est ainsi communément admis que l’hématocrite influence de façon significative les processus d’hémostase. Cependant les effets spécifiques des variations de l’hématocrite apparaissent comme peu clairs et parfois contradictoires, soulignant la nécessité d’études complémentaires. La compréhension de l’influence de l’hématocrite sur ces processus est essentielle d’un point de vue clinique puisque de nombreux patients souffrant de pathologies impliquant une diminution ou une augmentation anormale de l’hématocrite (anémies hémolytiques et polyglobulies, respectivement) présentent un risque thrombotique accru. Ce point est d’autant plus crucial que certaines de ces affections combinent des altérations quantitatives, liées aux variations de l’hématocrite, et des anomalies qualitatives des GRs, susceptibles d’amplifier les perturbations hémodynamiques et hémostatiques.
Impact de la déformabilité érythrocytaire sur les différentes phases de l’hémostase
Comme évoqué précédemment, les GRs déformables tendent à se déplacer au centre du vaisseau, contrairement aux GRs rigides, qui circulent près des parois. Ce phénomène possède deux effets paradoxaux sur l’initiation de la formation du caillot. D’une part, les GRs proches des parois entrent en compétition avec les plaquettes, réduisent l’épaisseur de la couche de déplétion et limitent l’adhésion plaquettaire à l’endothélium. D’autre part, la proximité des GRs avec la paroi exerce un effet abrasif qui active les cellules endothéliales et augmente l’expression de protéines d’adhérence vasculaire.
Plus tard, les GRs sont incorporés dans les caillots sanguins aussi bien artériels que veineux, puisqu’ils sont piégés par le maillage de fibrine au moment de la coagulation. Lors de la contraction physiologique du caillot qui s’ensuit, les GRs piégés se déforment pour prendre la forme de polyhédrocytes (1). Ce phénomène, permis par la forte capacité des GRs à se déformer, est indispensable pour augmenter la fermeté et la stabilité du caillot ainsi que pour rétablir le flux sanguin pendant la cicatrisation vasculaire, tout en colmatant la brèche. Une étude réalisée dans un modèle murin d’hémophilie A a confirmé l’importance de cette capacité de déformabilité et de formation de polyhédrocytes, puisqu’un traitement substitutif en FVIII permettait de rétablir le nombre de polyhédrocytes présents dans le caillot, ainsi que de normaliser le temps de saignement (17). De la même façon, la présence de GRs rigides (GRs drépanocytaires ou rigidifiés artificiellement avec un agent chimique) réduit fortement la capacité de contraction des caillots sanguins générés ex vivo (18). En revanche, ces observations s’opposent aux résultats d’une étude récente montrant que l’activation pharmacologique du canal érythrocytaire mécanosensible Piezo1, connue pour causer une déshydratation cellulaire par activation du canal Gardos et une réduction de la déformabilité érythrocytaire, augmentait la compaction des GRs au sein du caillot (19). Les auteurs suggèrent un effet médié par la modification des propriétés de la membrane des GRs à la suite de l’activation du canal Piezo 1. Des études supplémentaires sont nécessaires pour essayer de séparer les effets purement rhéologiques des effets du phénotype membranaire érythrocytaire sur la coagulation.
La déformabilité des GRs influence aussi la lyse des caillots sanguins. Il est admis que leur capacité à se déformer et à adopter une forme de polyhédrocytes rend le caillot plus imperméable aux agents lytiques au moment de sa contraction, augmentant ainsi sa résistance à la fibrinolyse (20). Cependant, d’autres travaux réalisés in vitro indiquent que les caillots les plus fermes lysent plus rapidement lorsqu’ils sont formés en présence d’agents lytiques, car la fibrine y retient davantage l’agent lytique durant la contraction (1). Bien que controversé et seulement partiellement élucidé, le rôle de la déformabilité érythrocytaire dans l’hémostase et en particulier au moment de la contraction des caillots semble majeur et pourrait constituer une nouvelle cible thérapeutique.
Impact de l’agrégation érythrocytaire sur les différentes phases de l’hémostase
Comme nous l’avons évoqué précédemment, les zones de faible vitesse de cisaillement sont plus propices à la formation d’agrégats de GRs mais ces agrégats peuvent également subsister dans des gros vaisseaux où la vitesse de cisaillement est modérée. Dans ce cas-là, les agrégats se déplacent au centre des vaisseaux sanguins et favorisent la margination et l’adhésion aux parois des autres éléments figurés. En revanche, si les vitesses de cisaillement sont élevées, les phénomènes d’agrégation érythrocytaire semblent cette fois induire une diminution de la margination et de l’adhésion des plaquettes (21).
Si l’agrégation érythrocytaire impacte le caillot dès sa formation, ses effets sur la dynamique globale des processus de coagulation sont également de plus en plus étudiés. Le fibrinogène, en tant que médiateur majeur de l’agrégation érythrocytaire, joue un rôle central dans ce processus, d’autant plus que son augmentation pathologique est associée à un risque thrombotique accru. En effet, une élévation de la concentration plasmatique en fibrinogène engendre une augmentation de la formation de rouleaux de GRs (par l’intermédiaire des mécanismes que nous avons détaillés précédemment), conduisant à une augmentation de la viscosité sanguine propice à la stase sanguine. Ce lien a été renforcé par une récente étude qui a mis en évidence un profil hypercoagulable évalué par thromboélastométrie rotative chez des patients atteints de COVID-19, en lien avec une forte augmentation de l’agrégation érythrocytaire associée à une hyperfibrinogénémie (22). Le niveau d’agrégation érythrocytaire était positivement corrélé à la fermeté des caillots sanguins formés in vitro et négativement avec le temps de formation de ces caillots. De plus, le temps d’hospitalisation des patients et la présence de lésions pulmonaires étaient positivement corrélés au niveau d’agrégation érythrocytaire (22). Ces observations suggèrent que l’augmentation de l’agrégation érythrocytaire contribue directement aux propriétés mécaniques du caillot, un effet pouvant s’expliquer par le rôle du fibrinogène comme médiateur des interactions inter-cellulaires favorisant à la fois la liaison inter-GRs et la formation d’agrégats plaquettaires. Ces liaisons sont médiées par des récepteurs présents au niveau de la membrane des GRs tels que des intégrines, le CD47, ou encore la protéine αIIbβ3 et peuvent favoriser les processus de coagulation (23) (Figure 4).
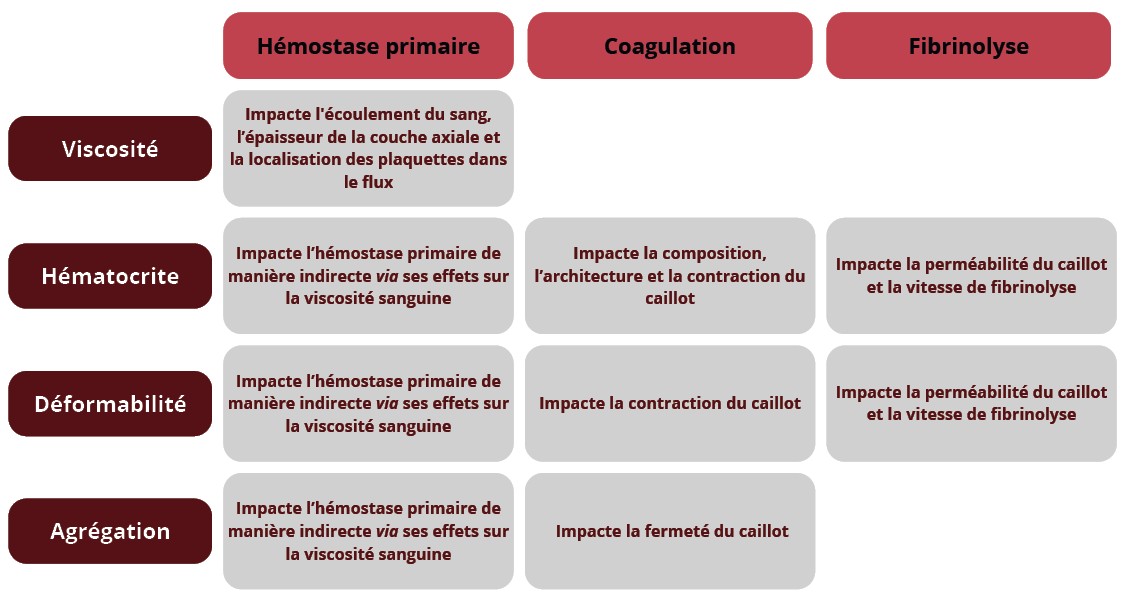
Figure 4 : Effet des variations des différentes propriétés des globules rouges sur les trois phases de l’hémostase.
Figure 4: Effect of variations in different red blood cell properties on the three phases of hemostasis.
IMPACT DES PROPRIÉTÉS MEMBRANAIRES ÉRYTHROCYTAIRES ET DES MOTIFS MOLÉCULAIRES ASSOCIÉS AUX DOMMAGES D’ORIGINE ÉRYTHROCYTAIRE SUR L’HÉMOSTASE
Phénotype membranaire des globules rouges et hémostase
Phosphatidylsérine
Dans les GRs, la phosphatidylsérine (PS) est un phospholipide anionique majoritairement confiné sur le feuillet interne de la membrane plasmique. Chez un individu sain, moins de 0,5 % des GRs exposent naturellement la PS à leur surface. Celle-ci sert de signal de reconnaissance pour les macrophages, ce qui facilite l’élimination des GRs vieillissants ou endommagés au niveau de la rate. La PS peut être transloquée et exposée de manière anormalement élevée sur la face externe de la membrane des GRs, c’est notamment le cas dans la drépanocytose, la thalassémie, ou en cas de stress oxydatif accru. Cette augmentation de l’exposition de la PS peut avoir pour origine un influx de Ca2+ intra-érythrocytaire provoqué par un dérèglement de l’activité de canaux cationiques, une altération des propriétés biophysiques du GR, une inflammation ou la présence excessive d’espèces réactives de l’oxygène (ROS) (24). La PS exposée sert alors de site d’ancrage supplémentaire, fournissant une surface procoagulante où les facteurs Va et Xa vont pouvoir s’assembler en présence de Ca2+ pour permettre la génération de thrombine. Il a été montré que le pourcentage de GRs exposant de la PS était positivement corrélé à des marqueurs de génération de thrombine et de fibrinolyse, chez des patients atteints de drépanocytose (25).
Molécules d’adhérence érythrocytaire
Au-delà de son rôle pro coagulant, la PS exposée sur la membrane externe des GRs favorise leur adhérence à l’endothélium, via des interactions indirectes impliquant des protéines plasmatiques et des récepteurs endothéliaux de reconnaissance de la PS. Dans certaines pathologies dont la drépanocytose, les GRs des patients sont également caractérisés par la présence accrue d’autres molécules membranaires d’adhérence, ce qui induit une augmentation des interactions entre les GRs et les autres composants de la circulation sanguine. Par exemple, il a été démontré qu’à la suite d’une lésion vasculaire, les GRs des patients drépanocytaires peuvent se lier à la matrice sous-endothéliale, en partie grâce à une interaction impliquant Lu/BCAM (26). Dans d’autres études, il a été observé la présence importante d’agrégats érythro-plaquettaires, impliquant des interactions entre le CD36 et la thrombospondine (27), ou ICAM4 (GRs) et αIIbβ3 (plaquettes). Le potentiel pro-adhésif des GRs dans certaines pathologies pourrait alors participer de façon significative à l’état procoagulant observé dans celles-ci.
Hémolyse et microparticules
L’hémolyse est un processus de destruction des GRs. On distingue l’hémolyse extravasculaire, réalisée par les macrophages de la rate et du foie, qui permet l’élimination des GRs sénescents ou abîmés, et l’hémolyse intravasculaire, qui se produit directement dans la circulation sanguine et qui mène à la libération, délétère, du contenu intra-érythrocytaire au sein de celle-ci. L’hémolyse intravasculaire est un processus physiopathologique observé dans les hémoglobinopathies (drépanocytose, thalassémies),les pathologies de la membrane érythrocytaire (sphérocytose héréditaire, ovalocytose, stomatocytose héréditaire, etc.), les enzymopathies érythrocytaires (déficit en pyruvate kinase, etc.) et les canalopathies (mutation Gardos, mutation Piezo1, etc.). L’accumulation d’hémoglobine et d’hème libre (considérés comme des DAMPs d’origine érythrocytaire) dans le plasma de patients ayant une anémie hémolytique, est susceptible de contribuer à l’activation de l’hémostase via plusieurs mécanismes :
• l’hémoglobine et l’hème libres majorent le stress oxydatif et l’inflammation, deux conditions favorisant l’activation des plaquettes ;
• l’hémoglobine libre réduit la biodisponibilité du monoxyde d’azote en favorisant sa transformation en nitrate, conduisant à une réduction de la vasodilatation et à une augmentation de l’activation et de l’agrégation plaquettaire;
• l’hémoglobine libre peut se fixer aux récepteurs plaquettaires GP1bα et P2Y12, et favoriser l’activation, l’apoptose et l’agrégation plaquettaire (28) ;
• quand les contraintes de cisaillement sont importantes, l’hémoglobine libre entre en interaction avec le VWF augmentant son affinité avec le complexe GPIb-IX-V à la surface des plaquettes, contribuant alors à leur activation mais aussi à une liaison massive au fibrinogène induisant la formation du thrombus (29) ;
• l’hème libre provoque également l’activation et la dégranulation plaquettaire via sa liaison au récepteur TLR4 et la génération de ROS mitochondriaux (30).
Enfin, la libération d’ADP lors de la lyse érythrocytaire peut engendrer une activation plaquettaire.
Les dommages membranaires et les processus de sénescence érythrocytaire dans la plupart des pathologies érythrocytaires s’accompagnent également d’une émission accrue de microparticules (MPs) par bourgeonnement membranaire. La protéine bande 3, présente à la surface des GRs se compose d’un domaine transmembranaire impliqué dans l’échange d’anions (comme le bicarbonate) et d’un domaine cytoplasmique, essentiel au maintien de la structure et de la stabilité membranaire des érythrocytes. Elle interagit avec les protéines du cytosquelette et joue un rôle dans la déformabilité érythrocytaire puisque son altération induit une désorganisation du cytosquelette.
Par exemple, le processus de clusterisation de la bande 3 est impliqué dans la formation de MPs, qui sont particulièrement riches en PS favorisant ainsi l’activation de la coagulation. Ces MPs d’origine érythrocytaire sont susceptibles de contenir d’autres molécules procoagulantes (la scramblase phospholipidique I, le précurseur du plasminogène, le précurseur de la chaîne bêta du fibrinogène, le précurseur du composant C9 du complément et la β2-glycoprotéine I) et peuvent alors favoriser à la fois l’activation de la voie extrinsèque et celle de la voie intrinsèque de la coagulation (31). Ainsi, l’émission accrue de MPs d’origine érythrocytaire apparaît comme un mécanisme clé reliant les altérations membranaires des GRs à l’état prothrombotique observé dans de nombreuses pathologies.
CONCLUSION
En définitive, les GRs, bien plus que de simples transporteurs d’oxygène, se révèlent acteurs clés des processus d’hémostase et de fibrinolyse. Les données expérimentales in vitro et in vivo, ainsi que les études cliniques, montrent que les caractéristiques rhéologiques du sang ainsi que les propriétés biophysiques et membranaires des GRs modulent ces processus complexes. Si des travaux supplémentaires restent nécessaires pour élucider tous leurs mécanismes, leur rôle émergent ouvre la voie à de nouvelles stratégies thérapeutiques pour prévenir et traiter les pathologies associées à un risque thromboembolique élevé.
Ainsi, l’histoire des GRs continue de se dévoiler, de la simple cellule au régulateur complexe de l’équilibre hémostatique.
POINTS CLÉS À RETENIR
• Les GRs participent activement à l’hémostase et à la thrombose, influençant la coagulation par leur quantité (hématocrite) et leurs propriétés rhéologiques (déformabilité, agrégation).
• L’exposition de la phosphatidylsérine, l’expression de molécules d’adhérence et l’émission de MPs d’origine érythrocytaire modulent la formation, la contraction et la lyse des caillots.
• Les altérations des GRs (quantitatives ou qualitatives) sont associées à un risque accru d’événements thrombotiques, faisant des GRs une cible thérapeutique potentielle.
Liens d’intérêts : les auteurs déclarent ne pas avoir de lien d’intérêt en rapport avec cet article.

