ÉDITION SPÉCIALE EAHAD 2026
19th Annual Congress of the European Association for Haemophilia and Allied Disorders
Du 3 au 6 février 2026, Dublin
Avec le soutien institutionnel
![]()
![]()
D’après les communications orales de :
– Y. Sakurai et al., VGA039, a protein S-targeting monoclonal antibody, restores hemostasis in von Willebrand disease patient blood in an ex vivo bleeding model. Abstract SLAM session
– G. Yamaguti-Hayakawa et al., Subcutaneous, every-four-week maintenance dosing of a novel protein S antibody is well-tolerated and substantially reduces bleeding rates : Results from a phase ½ multi-dose study of VGA039 in patients with von Willebrand disease. Abstract SLAM session
19th Annual Congress of the European Association of Haemophilia and Allied Disorders 2026, 3-6 February
Antoine Babuty, Nantes
La maladie de Willebrand (VWD) est la pathologie hémorragique constitutive la plus fréquente. Le VGA039 est un anticorps monoclonal de type IgG4, entièrement humanisé ciblant la protéine S. Il limite l’activation de la protéine C activée au niveau des cellules endothéliales, et du TFPIα à la surface des plaquettes (Figure 1). Il n’induit pas de déficit profond en protéine S et n’inhibe pas l’action du TFPIβ qui permet de limiter l’expansion du caillot au niveau des sites de lésion vasculaire.
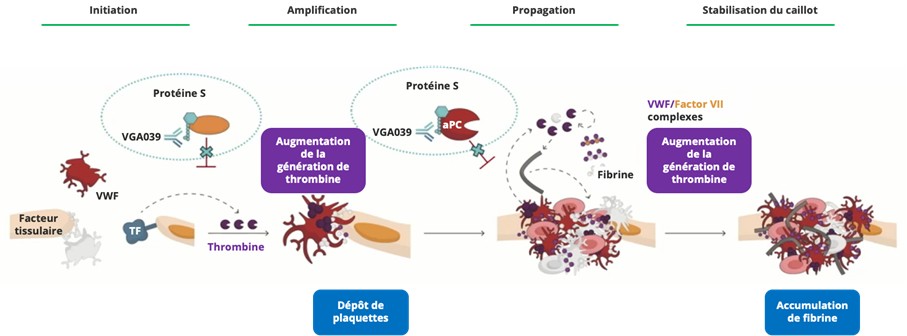
Figure 1 : Effets de VGA039 et conséquences sur l’hémostase
Des études in vitro ont été réalisées sur un modèle de vaisseau endothélialisé, à haute condition flux (1500 s-1) avec du sang de patient atteint de VWD de type 3. Une ponction permettait de reproduire une lésion vasculaire. Le VGA039 diminuait le temps de saignement et accélérait le dépôt des plaquettes ainsi que l’accumulation de fibrine (Figure 2), de façon significative. A noter que ces effets n’ont toutefois pas été comparés à ceux résultant d’un apport de facteur Willebrand exogène.
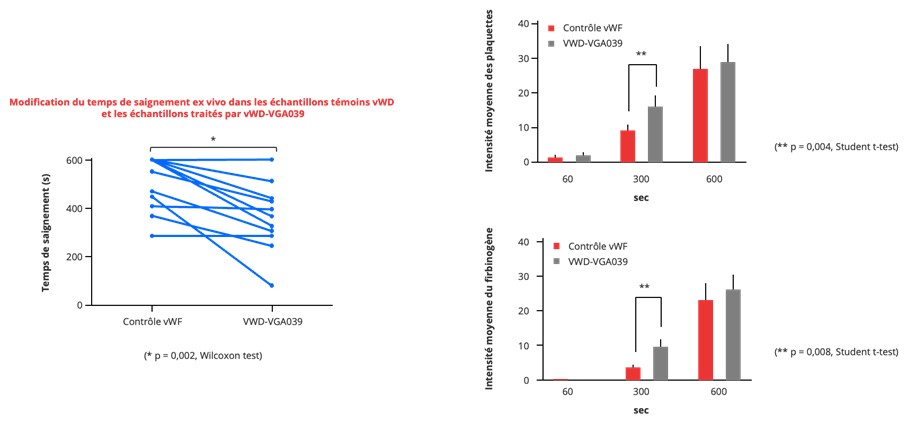
Figure 2 : Effets du VGA039 sur le temps de saignement et le dépôt de plaquettes ou de fibrinogène après lésion vasculaire sur vaisseau isolé et perfusé avec du sang de patients avec une VWD type 3
L’étude VIWID 3 est une étude ouverte de phase I/II ayant évalué l’administration de doses multiples de VGA039 par voie sous-cutanée. Elle a inclus des patients atteints de tout type de VWD symptomatique de 12 à 60 ans, traités ou non par une prophylaxie avec du facteur Willebrand et exclut les patients avec un taux de FVIII normal, des antécédents thromboemboliques ou de pathologie pro-thrombotique et l’utilisation de traitement contenant des œstrogènes. La sécurité, les profils pharmacocinétiques/pharmacodynamiques (PK/PD) et l’efficacité du VGA039 sur les saignements ont été évalués. Huit patients, avec autant d’hommes que de femmes et tous types de VWD ont été traités 17 semaines. Six patients ont reçu une dose de charge puis 225 mg toutes les 4 semaines. La majorité des patients de ces patients ont atteint la cible attendue de 25 µg/ml, à l’exception d’un seul cas de plus de 100 kg. Les patients avec un poids de moins de 60 kg présentaient des taux circulant de médicament plus élevés, ce qui a conduit à adapter la dose selon le poids dans une deuxième cohorte. Aucun patient n’a arrêté le traitement, il n’y a pas eu d’évènement thromboembolique, ni de réaction aux sites d’injections et il n’y avait pas d’augmentation significative des D-dimères. Deux évènements indésirables de grade 2 et liés au traitement à type de céphalées ont été rapportés chez un patient. Un évènement indésirable grave non lié au traitement à type de saignement gastro intestinal, a été décrit chez un autre patient avec de nombreux antécédents. Ce traitement a permis une réduction médiane des saignements annualisés de 81% (Figure 3).
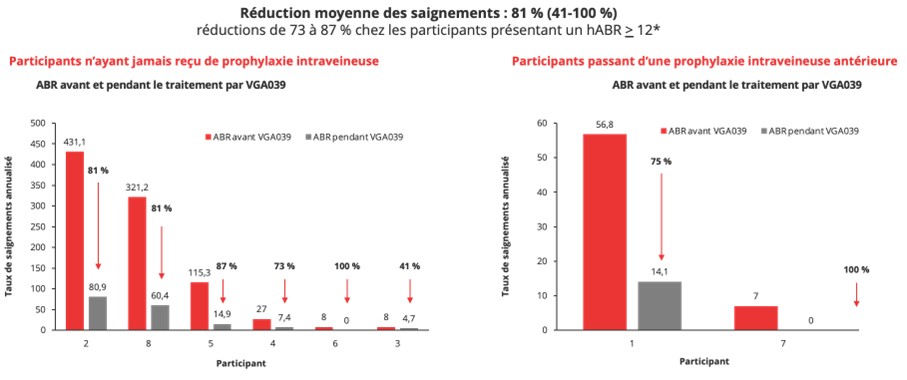
Figure 3 : Efficacité de VGA030 sur le saignement chez des patients atteints de maladie de Willebrand
Toutefois, il faut souligner que cette étude a inclus des profils de patients présentant de nombreux saignements.
A ce titre, l’histoire d’un malade âgé de 50 ans avec une symptomatologie hémorragique digestive récidivante liée à une angiodysplasie malgré une prophylaxie intensive et de l’acide tranexamique a été mise en avant. Le VGA039 a en effet permis une réduction des saignements de 96 % avec un arrêt complet de la prophylaxie en 15 jours.
Néanmoins, le bénéfice et la bonne tolérance de cette nouvelle thérapie demande à être confirmée et tous les patients inclus sont désormais entrés dans la phase d’extension de l’étude, qui est toujours en cours de recrutement.
Attention : ceci est un compte-rendu et/ou résumé des communications de congrès dont l’objectif est de fournir des informations sur l’état actuel de la recherche ; ainsi, les données présentées sont susceptibles de ne pas être validées par les autorités françaises et ne doivent donc pas être mises en pratique.
Ce compte-rendu a été réalisé sous la seule responsabilité du coordinateur, des auteurs et du directeur de la publication qui sont garants de l’objectivité de cette publication.

